Dẫn 36g hỗn hợp khí gồm CO và H2 đi từ từ qua139,2g bột sắt Fe3O4 đun nóng ở nhiệt độ caoo, thu dc m gam sắt và 74,4 g hỗn hợp CO2 và H2O. Tính khối lượng sắt thu dc sau phản ứng, biết phản ứng vừa đủ .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH:
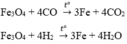
Áp dụng định luật bảo toàn khối lượng, ta có:
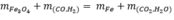
m_Fe=m=139,2+36-74,4=100,8 gam

Theo gt ta có: $n_{Fe_3O_4}=0,05(mol)$
$Fe_3O_4+4H_2\rightarrow 3Fe+4H_2O$
Ta có: $n_{H_2}=0,05.4=0,2(mol)\Rightarrow V_{H_2}=4,48(l)$

\(n_{CO\left(bđ\right)}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(CO+O_{oxit}\rightarrow CO_2\)
\(n_{CO}=n_Y=0.25\left(mol\right)\)
\(M_Y=18.8\cdot2=37.6\left(\dfrac{g}{mol}\right)\)
Bảo toàn khối lượng :
\(m_A=37.6\cdot0.25+12.32-0.25\cdot28=14.72\left(g\right)\)

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\\ Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2\)
Theo PTHH : \(n_{Zn} = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\)
\(\Rightarrow n_{Fe_2O_3} = \dfrac{35,5-0,3.65}{160} = 0,1\\ \Rightarrow n_{HCl} = 2n_{Zn} + 6n_{Fe_2O_3} = 0,3.2 + 0,1.6 = 1,2(mol)\\ \Rightarrow m_{HCl} = 1,2.36,5 = 43,8(gam)\)
b)
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\)
Gọi \(n_{CuO} = a;n_{Fe_2O_3} = b\)
\(\left\{{}\begin{matrix}80a+160b=19,6\\a+3b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,135\\b=0,055\end{matrix}\right.\)
Vậy :
\(\left\{{}\begin{matrix}n_{Cu}=0,135\\n_{Fe}=0,055.2=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,135.64=8,64\left(gam\right)\\m_{Fe}=0,11.56=6,16\left(gam\right)\end{matrix}\right.\)

Tham khảo :
PTHH :
Fe3O4 + 4CO -----> 3Fe + 4CO2
Fe3O4 + 4H2 -----> 3Fe + 4H2O
Phản ứng đủ
Theo Định luật BTKL ta có :
mFe3O4 + mhh (khí) - mCO2 - mH2O = mFe
=> 139,2 + 36 - 74,4 = mFe
=> 100,8 (g) = mFe
Vậy khối lượng sắt thu được sau phản ứng là 100,8 (g)
Tham khảo:
m_Fe=m=139,2+36-74,4=100,8 gam

a) Gọi \(n_{Cu}=a\left(mol\right)\rightarrow n_{Fe}=\dfrac{3}{2}a=1,5a\left(mol\right)\)
PTHH:
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
a<------a<------a
\(Fe_3O_4+4H_2\xrightarrow[]{t^o}3Fe+4H_2O\)
0,5a<-----2a<------1,5a
\(\rightarrow80a+0,5a.232=39,2\\ \Leftrightarrow a=0,2\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}m_{CuO}=0,2.80=16\left(g\right)\\m_{Fe_3O_4}=0,5.0,2.232=23,2\left(g\right)\end{matrix}\right.\)
b) \(V_{H_2}=\left(0,2.2+0,2\right).22,4=13,44\left(l\right)\)

Đáp án D.
Ta có: mO = 0,32 (g) ⟹ nO = 0 , 32 16 = 0,02 (mol) nên số mol của hỗn hợp CO, H2 cũng bằng 0,02 (mol) ⟹ V = 0,02.22,4 = 0,448 (l).
Theo định luật bảo toàn khối lượng, m = 16,8 – 0,02.16 = 16,48 (g).

a) Đặt \(n_{Cu}=a\left(mol\right)\)
\(\rightarrow n_{Fe}=1,5a\left(mol\right)\)
PTHH:
\(Fe_3O_4+4H_2\xrightarrow[]{t^o}3Fe+4H_2O\)
0,5a<---2a<------1,5a
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
a------>a------->a
Theo bài ra, ta có PT: \(0,5a.232+80a=39,2\)
\(\Leftrightarrow a=0,2\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_3O_4}=0,5.0,2.232=23,2\left(g\right)\\m_{CuO}=0,2.80=16\left(g\right)\end{matrix}\right.\)
b) \(V_{H_2}=\left(0,2.2+0,2\right).22,4=13,44\left(l\right)\)
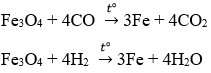
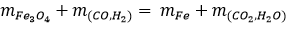
Fe3O4 + 4CO → 3Fe + 4CO2
Fe3O4 + 4H2 → 3Fe + 4H2O
Theo định luật bảo toàn khối lượng
=> mFe3O4 + mCO + H2 = mFe + mCO2 + H2O
=> 139,2 + 36 = mFe + 74,4
=> mFe = 100,8 ( gam )
=> Khối lượng Fe thu được sau phản ứng là 100,8 gam
PTHH :
Fe3O4 + 4CO -----> 3Fe + 4CO2
Fe3O4 + 4H2 -----> 3Fe + 4H2O
Phản ứng đủ
Theo Định luật BTKL ta có :
mFe3O4 + mhh (khí) - mCO2 - mH2O = mFe
=> 139,2 + 36 - 74,4 = mFe
=> 100,8 (g) = mFe
Vậy khối lượng sắt thu được sau phản ứng là 100,8 (g)