Hấp thụ toàn bộ x mol CO2 vào dd chứa 0,03mol Ca(OH)2 được 2g kết tủa. Tìm giá trị x
Help me
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
Ta có : n CaCO3 = 2/100 = 0,02 mol ≠ n CaCO3 =0,03 mol
Xét 2 Trường hợp :
TH1 : chỉ xảy ra phản ứng tạo CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,02 0,02
=> n CO2 = n CaCO3 =0,02 mol
TH2 : xảy ra 2 phản ứng tạo muối CaCO3và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,02 0,02
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,02 0,01
Theo phản ứng (1)và (2) : n CO2 p/ứ= 0,02 + 0,02 = 0,04 mol
=> Đáp án A
CÁCH khác : sử dụng phương pháp đồ thị :
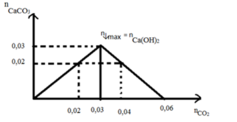
Dựa vào đồ thị => n CO2 = 0,02 mol hoặc 0,04 mol

nCaCO3 = 2/100 = 0,02 mol
* Trường hợp 1 : CO2 hết
Ca(OH)2 + CO2 = CaCO3 + H2O
nCO2 = nCaCO3 = 0,02 mol => VCO2 = 0,02.22,4 = 0,448 lit
** Trường hợp 2 : CO2 dư
Ca(OH)2 + 2CO2 = Ca(HCO3)2
x...............2x mol
Ca(OH)2 + CO2 = CaCO3 + H2O
y...............y.........y mol
nCaCO3 = y = 0,02
nCa(OH)2 = x + y = 0,03 => x = 0,03 - 0,02 = 0,01
=> nCO2 = 2x + y = 2.0,01 + 0,02 = 0,04 mol => VCO2 = 0,04.22,4 = 0,896 lit
khối lượng kết tủa chính là của CaC03 => số mol CaC03 =0,02 mol
sau đó viết phương trình pư

Đáp án C
nOH- = n NaOH + 2n Ca(OH)2 = 0,05 mol
n CO2 = 0,672/22,4 = 0,03 mol
CO2 + OH- → HCO3-
0,03 → 0,03 → 0,03
HCO3- + OH- → CO32- + H2O
0,02 ← 0,02 0,02
Ca2+ + CO32-→ CaCO3↓
0,0125 → 0,0125 → 0,0125
=> x = 0,0125.100 = 1,25 g

Đáp án C
nOH- = n NaOH + 2n Ca(OH)2 = 0,05 mol
n CO2 = 0,672/22,4 = 0,03 mol
CO2 + OH- → HCO3-
0,03 → 0,03 → 0,03
HCO3- + OH- → CO32- + H2O
0,02 ← 0,02 → 0,02
Ca2+ + CO32- → CaCO3↓
0,0125 0,02 → 0,0125
⇒ x = 0,0125.100 = 1,25 g

Chọn D
nCO2 dùng ở 2 thí nghiệm là như nhau nhưng TN2 cho nhiều BaCO3 hơn TN1
Þ Trong dung dịch sau phản ứng của TN1 còn Ba2+ cùng với CO32− hoặc HCO3-
Þ Dung dịch sau phản ứng của TN1 chỉ có Ba(HCO3)2.
Vậy ở TN1 bản chất là giống thí nghiệm 1 tạo ra 0,1 mol BaCO3 và dung dịch có a – 0,1 mol Ba(HCO3)2
Lượng NaOH thêm vào là a > nBa(HCO3)2 Þ Toàn bộ Ba2+ đã kết tủa
Þ a – 0,1 = 0,1 Þ a = 0,2; BTNT.C Þ nCO2 = 0,1 + 0,1.2 = 0,3 Þ V = 6,72.
Ối ối bài này có trong đề thi vòng 1 này , cũng gần giống
Theo đề bai ta có : \(nCa\left(OH\right)2=0,03\left(mol\right)\) ; mkt = 2g
Ta có PTHH :
(1) \(Ca\left(OH\right)2+CO2->CaCO3\downarrow+H2O\)
=> mCaCO3 = 2 => nCaCO3 = \(\dfrac{2}{100}=0,02\left(mol\right)\)
Ta xét 2 TH
* TH 1 : số mol của Bazo dư => tính theo số mol của kết tủa
Theo PTHH ta có : nCO2 = nCaCO3 = 0,02 (mol)
=> x = nCO2 = 0,02 (mol)
* TH 2 : số mol của kết tủa dư ( tính theo số mol của bazo )
Theo PTHH 1 ta có :
nCO2 = nCa(OH)2 = 0,03 (mol)
nCaCO3 = nCa(OH)2 = 0,03 (mol)
Mà vì số mol ban đầu của kết tủa là 0,02 mol , số mol của kết tủa p/ư ở PTHH 1 là 0,03 mol nên => Chứng tỏ 0,01 mol kết tủa đã tiếp tục pản ứng với CO2
Ta có PTHH 2
\(CaCO3+CO2+H2O->Ca\left(HCO3\right)2\)
0,01mol........0,01mol
=> x = nCO2(1) + nCO2(2) = 0,03 + 0,01 = 0,04 (mol)
Vậy.............