1)Cho 100ml FezCl2 1M tác dụng với dung dịch NaOH lấy dư thu được một chất kết tủa trắng , xanh và dung dịch A. Lọc tách kết tủa rồi đem nung nóng thu được một chất kết tủa màu đen . Cho chất rắn đó vào ống sứ , nung đỏ rồi cho khí CO đi qua đến khi phản ứng kết thúc thu được kim loại màu trắng bạc . Tính khối lượng kim loại đó .
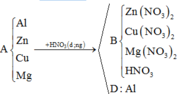
2)Hòa tan hoàn toàn 18,4g hh gồm sắt và sắt (II) oxit=300ml dd H2SO4 1M coa khối lượng riêng d=1,65 g/ml tác dụng vừa đủ
a)Tính thành phần phần trăm theo khối lượng mỗi chất hh ban đầu .
b)Tính C% cuả muối tạo thành dd sau phản ứng

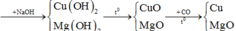
gọi x la so mol cua Fe
y la so mol cua FeO
\(n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\)
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2
de: x \(\rightarrow\) x \(\rightarrow\) x \(\rightarrow\) x
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2
de: y \(\rightarrow\) y \(\rightarrow\) y \(\rightarrow\) y
Ta co: 56x + 72y = 18,4
x + y = 0,3
\(\Rightarrow\) x = 0,2 y = 0,1
a, \(m_{Fe}=56.0,2=11,2g\)
\(m_{FeO}=72.0,1=7,2g\)
\(\%m_{Fe}=\dfrac{11,2}{18,4}.100\%\approx60,87\%\)
\(\%m_{FeO}=100-60,87\approx39,13\%\)
b, \(m_{FeSO_4}=152.\left(0,1+0,2\right)=45,6g\)
\(m_{dd}=18,4+300.1,65-0,4=513g\)
\(C\%=\dfrac{45,6}{513}.100\%\approx8,89\%\)