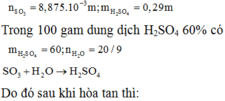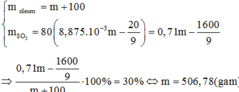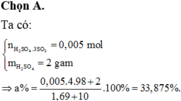Có một loại oleum X trong đó SO3 chiếm 71% theo khối lượng. Lấy a gam X hòa tan vào b gam dung dịch H2SO4 c% được dung dịch Y có nồng độ d%. Lập biểu thức tính d theo a, b, c.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Oleum H2SO4.nSO3 có 0,71a gam SO3 và 0,29a gam H2SO4
Sau khi thả oleum vào dd H2SO4, SO3 tan hết tạo H2SO4
\(n_{SO3}=\frac{71a}{8000}=n_{H2SO4}\)
\(\rightarrow m_{H2SO4}=0,86975a\left(g\right)\)
Trong b gam dd H2SO4 C% có 0,01bc gam H2SO4
Tổng \(m_{H2SO4}=0,86975a+0,01bc\) gam H2SO4
\(m_{dd_Y}=a+b\left(g\right)\)
\(\rightarrow d=\frac{100\left(0,86975a+0,01bc\right)}{a+b}\)
\(=\frac{86,975a+bc}{a+b}\)

H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé

Đáp án : C
Xét 100g Oleum có 70g SO3 và 30g H2SO4
Khi hòa tn vào nước thu được dung dịch có H2SO4 chiếm 80%
=> SO3 chiếm 20%
n S = n H 2 S O 4 + n S O 3 = 1,18 mol
Dung dịch sau :
⇒ n H 2 S O 4 = 0 , 9 m o l
=> n H 2 S O 4 m ớ i = n H 2 S O 4 s a u - n H 2 S O 4 đ ầ u = 0 , 6 m o l = n H 2 O
=> m H 2 O = 10,8g

Gọi oleum X : H2SO4.nSO3
SO3 chiếm 71% theo khối lượng
\(\Rightarrow\) %SO3 = 80n/80n+98 = 71/100 = 0,71
\(\Leftrightarrow\) 80n = 0,71(80n+98)
\(\Leftrightarrow\) 23,2n = 69,58 \(\Leftrightarrow\) n = 3
Vậy công thức oleum là H2SO4.3SO3
_ Lấy 8,45 g X vào 20 g dd H2SO4 10%
\(\Rightarrow\) n X = 8,45/338 = 0,025 = n H2SO4 ( trong X )
\(\Rightarrow\) m H2SO4 = 0,025 . 98 = 2,45 g
\(\Rightarrow\) n SO3 = \(\dfrac{3.8,45}{338}\)= 0,075 mol
m ct(H2SO4 10%) = \(\dfrac{20.10}{100}\) = 2 g
_ SO3 trong X sẽ tác dụng với dd H2SO4 :
SO3 + H2O \(\rightarrow\) H2SO4
0,075..............0,075 (mol)
\(\Rightarrow\) m H2SO4(từ SO3) = 0,075 . 98 = 7,35 g
\(\Rightarrow\) m H2SO4(tạo thành) = 2 + 7,35 + 2,45 = 11,8 g
_ m dd sau pứ = 8,45 + 20 = 28,45 g
C% dd Y = \(\dfrac{11,8}{28,45}\).100% = 41,5%