Thành phần % về khối lượng của nguyên tố kim loại M trong hỗn hợp MCl2 và MSO4 là 21,1%. Tính thành phần % về khối lượng của nguyên tố Cl trong hỗn hợp trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích: Đáp án B
Xét trong 1 mol hỗn hợp :
- Gọi x là số mol MCl2 thì số mol của MSO4 là 1 - x
- Số mol của M : x + 1 - x = 1 mol
=> Khối lượng hỗn hợp là : (M + 71)x + (M + 96)(1 - x) = M + 96 - 25x
Phần trăm khối lượng M trong hỗn hợp là :
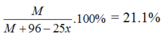
Ta có 0 < x < 1 => 18.9 < M < 25.7 => M = 24 (Mg)
=> x = 0.25 mol
=> khối lượng hỗn hợp là (24 + 71). 0,25 + (M + 96)(1 – 0,25) = 113.75g
=> %Cl = 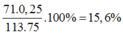

\(n_{NO_3} = n_N = \dfrac{52,39.14,43\%}{14} = 0,54(mol)\\ m_A = m_{kim\ loại} + m_{NO_3}\\ \Rightarrow m_{kim\ loại} = m_A - m_{NO_3} = 52,39 - 0,54.62 = 18,91(gam)\)

PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\) (1)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (2)
Ta có: \(\left\{{}\begin{matrix}\Sigma n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\\n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\Rightarrow n_{O_2\left(2\right)}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(1\right)}=1,425\left(mol\right)\) \(\Rightarrow n_{Mg}=2,85\left(mol\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{2,85\cdot24}{2,85\cdot24+2,7}\cdot100\%\approx96,2\%\)
\(\Rightarrow\%m_{Al}=3,8\%\)
\(n_{O_2} =\dfrac{33,6}{22,4} = 1,5(mol)\\ n_{Al} = \dfrac{2,7}{27} = 0,1(mol)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ n_{O_2} = \dfrac{1}{2}n_{Mg} + \dfrac{3}{4}n_{Al}\\ \Rightarrow n_{Mg} = 2,85(mol)\)
Vậy :
\(\%m_{Mg} = \dfrac{2,85.24}{2,85.24 + 2,7}.100\% = 96,2\%\\ \%m_{Al} = 100\% - 96,2\% = 3,8\%\)

Câu 1 :
Gọi CTHH muối là $M_3(PO_4)_2$
$\%P = \dfrac{31.2}{3M + 95.2}.100\% = 20\%$
$\Rightarrow M = 40(Ca)$
Vậy muối là $Ca_3(PO_4)_2$
Câu 2 :
Gọi CTHH muối là $M_3(PO_4)_2$
$\%M = \dfrac{3M}{3M + 95.2}.100\% = 38,7\%$
$\Rightarrow M = 40(Ca)$
Trong $CaCO_3$, $\%Ca = \dfrac{40}{100}.100\% = 40\%$

\(n_{CH_4}=\dfrac{2}{16}=0,125\left(mol\right)\)
\(PTHH:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(\left(mol\right)\) \(0,125\) \(0,25\)
Đặt \(\left\{{}\begin{matrix}n_{KMnO_4}=a\left(mol\right)\\n_{KClO_3}=b\left(mol\right)\end{matrix}\right.\)
\(\%m_K=26,68\left(\%\right)\Leftrightarrow\dfrac{39\left(a+b\right)}{158a+122,5b}=\dfrac{26,68}{100}\)
Lại có: \(0,5a+1,5b=0,25\) ( Cái này viết PTHH ra mới thấy)
\(\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{KMnO_4}=72\left(\%\right)\\\%m_{KClO_3}=28\left(\%\right)\end{matrix}\right.\)
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$n_{O_2} = 2n_{CH_4} = 2.\dfrac{2}{16} = 0,25(mol)$
Gọi $n_{KMnO_4} = a(mol) ; n_{KClO_3} = b(mol)$
Ta có :
$\dfrac{39(a + b)}{158a + 122,5b} = \dfrac{26,68}{100}(1)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{O_2} = 0,5a + 1,5b = 0,25(2)$
Từ (1)(2) suy ra a = 0,19 ; b = 0,1$
Ta có :
$\%m_{KMnO_4} = \dfrac{0,19.158}{0,19.158 + 0,1.122,5}.100\% = 71\%$
$\%m_{KClO_3} = 100\% - 71\% = 29\%$

\(a,n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\\
Fe+2HCl\rightarrow FeCl_2+H_2\\
n_{Fe}=n_{H_2}=0,2mol\\
m_{Fe}=0,2.56=11,2g\\
m_{Cu}=25-11,2=13,8g\\
b,\%m_{Fe}=\dfrac{11,2}{25}\cdot100=44,8\%\\
\%m_{Cu}=100-44,8=55,2\%\)
c, Gọi CTHH của sắt là \(Fe_xO_y\)
\(Fe_xO_y+yH_2\xrightarrow[t^0]{}xFe+yH_2O\\ \Rightarrow n_{Fe_xO_y}=n_{H_2}:y\\ \Leftrightarrow\dfrac{11,6}{56x+16y}=\dfrac{0,2}{y}\\ \Leftrightarrow11,6y=11,2x+3,2y\\ \Leftrightarrow11,6y-3,2y=11,2x\\ \Leftrightarrow8,4y=11,2x\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{8,4}{11,2}=\dfrac{3}{4}\\ \Rightarrow x=3;y=4\\ \Rightarrow CTHH:Fe_3O_4\)

có ở trên mạng nha
https://vn.answers.yahoo.com/question/index?qid=20120515074638AAH9nU1
http://viplam.net/diendan