Cho V(l) dung dịch axit clohidric 20% ( D=1,1g/ml) hòa tan hết với 10g canxi cacbonat thu được muối canxi clorua , nước và khí cacbon dioxit
a,Viết phương trình hóa học
b, Tính V dung dịch axit đã dùng
c, tính Khối lượng muối tạo thành
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

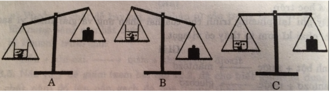
Chọn B. Vì khi cho đá vôi vào dung dịch axit clohiric có phản ứng sinh ra khí cacbon dioxit thoát ra ngoài làm cho khối lượng sẽ giảm đi.

\(n_{CaCO_3}=\dfrac{10}{100}=0,1\:mol\)
\(PTHH:\:CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
\(n_{HCl}=\dfrac{0,1.2}{1}=0,2\:mol\)
\(\Rightarrow m_{HCl}=0,2.36,5=7,3g\)

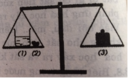
Sau khi phản cho (1) với (2) vào nhau xảy ra phản ứng
HCl + CaCO3 → CaCl2 + CO2 + H2O
Vì khí CO2 bị thoát ra nên khối lượng của bên cân chứa (1), (2) bị giảm xuống, cân nghiêng về phía có quả cân (3).

a)CaCO3 +2HCl-----> CaCl2 + CO2 +H2O
b) Ta có
n\(_{CaCO3}=\frac{10}{100}=0,1\left(mol\right)\)
Theo pthh
n\(_{CaCl2}=n_{CaCO3}=0,1\left(mol\right)\)
m\(_{CaCl2}=0,1.111=11,1\left(g\right)\)
c) Theo pthh
n\(_{CO2}=n_{CaCO3}=0,1\left(mol\right)\)
V\(_{CO2}=0,1.22,4=2,25\left(l\right)\)
Chúc bạn học tốt

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(n_{Zn}=\dfrac{0,65}{65}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,02\left(mol\right)\\n_{ZnCl_2}=0,01\left(mol\right)=n_{H_2}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{0,02}{0,05}=0,4\left(M\right)\\m_{ZnCl_2}=0,01\cdot136=1,36\left(g\right)\\V_{H_2}=0,01\cdot22,4=0,224\left(l\right)\end{matrix}\right.\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ b,n_{FeCl_2}=n_{H_2}=n_{Fe}=0,2(mol)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48(l)\\ m_{FeCl_2}=0,2.127=25,4(g)\)

a) Số mol canxi cacbonat tham gia phản ứng nCaCO3= 10/100 = 0,1 mol.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
Theo phương trình hóa học, ta có: nCaCl2= nCaCO3 = 0,1 mol.
Khối lượng của canxi clorua tham gia phản ứng: mCaCl2 = 0,1 . (40 + 71) = 11,1 g.
b) Số mol canxi cacbonat tham gia phản ứng: nCaCO3= 5/100 = 0,05 mol.
Theo phương trình hóa học, ta có: nCO2= nCaCO3 = 0,05 mol.
Thể tích khí CO2 ở điều kiện phòng là: VCO2 = 24 . 0,05 = 1,2 lít.

a) Pt: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b) nFe = \(\dfrac{11,2}{56}=0,2mol\)
Theo pt: nH2 = nFe = 0,2 mol
=> VH2 = 0,2.22,4 = 4,48lit
c) Theo pt: nHCl = 2nFe = 0,4 mol
=> mHCl = 0,4.36,5 = 14,6 g
=> C% = \(\dfrac{14,6}{73}.100\%=20\%\)
Theo đề bài ta có : nCaCO3 = \(\dfrac{10}{100}=0,1\left(mol\right)\)
a) Ta có PTHH :
CaCO3 + 2HCl \(\rightarrow\) CaCl2 + H2O + CO2\(\uparrow\)
0,1mol....0,2mol..........0,1mol
b) Ta có :
\(m_{\text{dd}HCl}=\dfrac{\left(0,2.36,5\right).100\%}{20\%}=36,5\left(g\right)\)
=> \(V_{\text{dd}HCl}=\dfrac{m}{D}=\dfrac{36,5}{1,1}\approx33,182\left(ml\right)\)
c) Khối lượng muối thu được là : mCaCl2 = 0,1.111 = 11,1 (g)
Vậy............
thks