Chọn 15,3gam oxit của một kim loại hóa trị II vào nước thu được 200gam dung dịch bazo có nồng độ 8,55% . Xác định công thức phân tử của oxit .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


đặt công thức oxit cần tìm là: XO
mX(OH)2= C%*mdd/100=8.55*200/100=17.1g
áp dụng bảo toàn khối lượng: mH2O=17.115.3=1.8g =>nH2O=1.8/18=0.1mol
pt: XO + H2O--> X(OH)2
0.1 0.1
MXO=15.3/0.1=153 g/mol
=> MX= MXO - MO2= 153-16=137
Vậy X là Ba. CTHH của oxit là BaO
Chúc em học tốt!!!:))

Gọi CTHH của oxit kim loại là RO
\(m_{R\left(OH\right)_2}=8,55\%.200=17,1\left(g\right)\)
Áp dụng định luật BTKL ta có: \(m_{H_2O}=17,1-15,3=1,8\left(g\right)\Rightarrow n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
PTHH: RO + H2O → R(OH)2
Mol: 0,1 0,1
\(\Rightarrow M_{RO}=\dfrac{15,3}{0,1}=153\left(g/mol\right)\)
⇒ MR = 153 - 16 = 137 (g/mol)
Vậy R là nguyên tố bari (Ba)

Cách 1: Đặt công thức hoá học của oxit là MO ⇒ công thức bazơ là M OH 2
MO + H 2 O → M OH 2
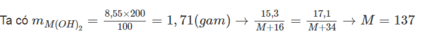
→ Công thức oxit là BaO.
Cách 2: m H 2 O ( p / u ) = m M OH 2 - m MO = 17,1 - 15,3 = 1,8(g)
MO + H 2 O → M OH 2
![]()
Công thức oxit là BaO

Chọn C
Đặt công thức hóa học của oxit là MO
PTHH:
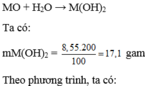
![]()
=> kim loại M là Ba
=> công thức oxit là BaO

a)Giả sử có 1 mol MO phản ứng
\(MO+2HCl\rightarrow MCl_2+H_2O\)
1----------->2----------->1----------->1
=> \(m_{ddHCl}=\dfrac{2.36,5}{10\%}=730\left(g\right)\)
\(m_{ddsaupu}=\left(M+16\right)+730=M+746\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{M+71}{M+746}.100=12,34\)
=> M=24 (Mg)
b) Giả sử có 1 mol M2On phản ứng
\(M_2O_n+2nHCl\rightarrow2MCl_n+nH_2O\)
1---------------->2n-------------->2----------->n
=> \(m_{ddHCl}=\dfrac{2n.36,5}{10\%}=730n\left(g\right)\)
\(m_{ddsaupu}=\left(2M+16n\right)+730n=2M+746n\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{2\left(M+35,5n\right)}{2M+746n}.100=12,34\)
Chạy nghiệm n=1,2,3
n=1 => M=12 (loại)
n=2 => M=24 (Mg)
n=3 => M=36 (loại)

bài 1:
Gọi oxit kim loai cần tìm là M
=> PTHH: MO + H2O ----> M(OH)2
m\(M\left(OH\right)_2\) = \(\dfrac{200.8,55\%}{100\%}=17,1\) (g)
=> n\(M\left(OH\right)_2\) = \(\dfrac{17,1}{M+34}\left(mol\right)\)
Theo PTHH: n\(MO\) = n\(M\left(OH\right)_2\) = \(\dfrac{17,1}{M+34}\left(mol\right)\)
=> m\(MO\) = \(\dfrac{17,1}{M+34}.\left(M+16\right)\)= \(\dfrac{17,1M+273,6}{M+34}=15,3\left(g\right)\)
=> 17,1M + 273,6 = 15,3M + 520,2
<=> 1,8M = 246,6
<=> M = 137
=> M là Ba
=> CTHH của oxit: BaO
2, CT: XO2
\(n_{Na_2XO_3}=\dfrac{18,9.400}{100}=75,6g\)
XO2 + 2NaOH\(\rightarrow\) Na2XO3 + H2O
pt: X + 32 46+ X +48 (g)
de: 38,4 75,6 (g)
Ta co: \(75,6\left(X+32\right)=38,4\left(94+X\right)\)
\(\Leftrightarrow75,6X+2419,2=38,4X+3609,6\)
\(\Leftrightarrow37,2X=1190,4\)
\(\Rightarrow X=32\left(đvC\right)\)\(\Rightarrow X\) là lưu huỳnh
CT: SO2
Gọi CTPT của oxit là RO
PTHH : RO + H2O \(\rightarrow\) R(OH)2
Theo đề bài ta có: \(n_{RO}=\dfrac{15,3}{R+16}\left(mol\right)\)
\(m_{R\left(OH\right)_2}=\dfrac{200.8,55}{100}=17,1\left(g\right)\)
\(\Rightarrow n_{R\left(OH\right)_2}=\dfrac{17,1}{R+34}\left(mol\right)\)
Theo phương trình : nRO = nR(OH)2
hay: \(\dfrac{15,3}{R+16}\) = \(\dfrac{17,1}{R+34}\)
\(\Leftrightarrow15,3R+520,2=17,1R+273,6\)
\(\Leftrightarrow1,8R=246,6\)
\(\Leftrightarrow R=137\)
=> R là Bari ( Ba)
Vậy CTPT của oxit là BaO