Cho các chất : nhôm,oxi,nước,đồng sunfat,sắt ,axit clohidric.Hãy điều chế đồng ,đồng (II)oxit ,nhôm clorua(bằng 2 phương pháp ) và sắt (II) clorua .Viết các PTPƯ.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn A.
(1) 2Fe + 3Cl2 → 2FeCl3
(2) Fe + S → t ° FeS
(3) 2FeO + 4H2SO4(đặc, nóng) → Fe2(SO4)3 + SO2 + 4H2O
(4) Fe + CuSO4 → FeSO4 + Cu
(5) Cu + 2FeCl3 → CuCl2 + 2FeCl2
(6) Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O

1)Tại sao nhôm hoạt động hơn sắt , đồng nhưng khi để các đồ vật bằng nhôm , sắt ,đồng ngoài không khí thì đồ vặt bằng nhôm rất bền ko bị hư hỏng , trái lại các đồ vật bằng sắt , đồng thì bị han rỉ ?
Trả lời : : Nhôm là kim loại hoạt động mạnh hơn Fe, Cu. Tuy nhiên các đồ vật bằng nhôm ở trong không khí vẫn không bị gỉ. Nguyên nhân là do lớp ngoài của Al đã tác dụng với O2 tạo một lớp oxit Al2O3 mỏng bảo vệ bên ngoài, ngăn không cho Al phản ứng với O2 nữa.
1. Do lớp ngoài của nhôm td với O2 tạo thành Al2O3 mỏng bảo vệ bên ngoài, ngăn ko cho Al td với oxi nữa.
2. Hòa tan hỗn hợp trong dung dịch HCl dư, sục tiếp khí O2 dư vào hh. Lọc, tách hất rắn sau pư làm khô được Ag nghuyên chất.
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Cu + 2HCl + O2 \(\rightarrow\) CuCl2 + H2O

4FeS2 + 11O2 ------to----> 2Fe2O3 + 8SO2
\(H_2O-^{đp}\rightarrow H_2+\dfrac{1}{2}O_2\)
\(2NaCl+2H_2O-^{đpddcmn}\rightarrow2NaOH+Cl_2+H_2\)
\(Cl_2+H_2-^{t^o}\rightarrow2HCl\)
Điều chế Fe(OH)2
\(Fe_2O_3+H_2-^{t^o}\rightarrow Fe+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Điều chế Fe(OH)3
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+H_2O\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
Điều chế Na2SO3
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
Điều chế NaHSO3
\(NaOH+SO_2\rightarrow NaHSO_3\)

+ Nam châm hút vật làm bằng sắt.
+ Nam châm không hút các vật làm bằng đồng, nhôm, nhựa, thủy tinh, gỗ.
Kết luận:
- Nam châm hút được các các vật được làm từ vật liệu từ (sắt, thép, cobalt, …)
- Nam châm không hút các vật không thuộc vật liệu từ (đồng, nhôm, …)

4Al + 3O2 \(\underrightarrow{t^o}\)2Al2O3
AlCl3 + 3NaOH \(\rightarrow\)Al(OH)3 + 3NaCl
Fe + H2SO4\(\rightarrow\)FeSO4 + H2
Al2O3 + 6HCl \(\rightarrow\)2AlCl3 + 3H2O
2Al + 3Cl2 \(\rightarrow\)2AlCl3
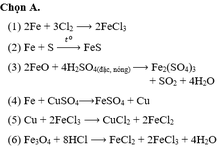
PTPƯ điều chế các chất trên :
- Điều chế Cu : Fe + CuSO4 \(\rightarrow\) FeSO4 + Cu .
- Điều chế CuO : 2Cu + O2 \(\underrightarrow{t^o}\) 2CuO.
- Điều chế AlCl3 bằng 2 phương pháp :
a) Al + 6HCl -> 2AlCl3 + 3H2.
b) 4Al + 3O2 \(\underrightarrow{t^o}\) 2Al2O3 ; Al2O3 + 6HCl -> 2AlCl3 + 3H2O
- Điều chế FeCl2 : Fe + 2HCl -> FeCl2 + H2.
Điều chế Cu : Fe + CuSO4 \(\rightarrow\) Cu + FeSO4
Điều chế CuO : 2Cu + O2 \(\rightarrow\) 2CuO
Điều chế AlCl3 :
1) 2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
2) 4Al + 3O2 \(\rightarrow\) 2Al2O3
Al2O3 + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Điều chế FeCl2 : Fe + 2HCl \(\rightarrow\) FeCl2 + H2