Cho hỗn hợp A gồm MgO và Al2O3. Chia A thành 2 phần hoàn toàn đều nhau, mỗi phần có khối lượng 19,88 gam. Cho phần 1 tác dụng với 200ml dung dịch HCl, đung nóng và khuấy đều. Sau khi kết thúc phản ứng , làm bay hơi cẩn thận hỗn hợp thu đc 47,38 g chất rắn khan. Cho phần 2 tác dụng với 400 ml dung dịch HCl đã dung ở thí nghiệm trên đun nóng, khuấy đều và sau khi kết thúc phản ứng cũng lại lam bay hơi hỗn hợp như trềnva cuối cùng thu đc 50,68 g chất rắn khan
a. Tính nồng độ mol của dd HCl đã dùng
b. Tính hàm lượng % theo khối lượng của mỗi oxit trong hỗn hợp A
P/s:Câu a giải định luật bảo toàn khối lượng dùm mình nha :)



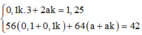
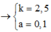
a) PTHH :
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O (1)
Al2O3 + 6HCl \(\rightarrow\) 2AlCl3 + 3H2O (2)
- Vì chia làm 2 phần bằng nhau nên : m(MgO + Al2O3)(Phần1) = m(MgO + Al2O3) (phần 2) = 19,88(g)
* Ta xét phần 1 :
Gọi nHCl(Pứ) = a(mol) \(\Rightarrow\) mHCl(Pứ) = 36,5a(g)
Theo PT(1)(2) \(\Rightarrow\) nH2O = 1/2 . nHCl(pứ) = 1/2 . a(g)
\(\Rightarrow\) mH2O= n .M = 1/2 . a . 18 = 9a(g)
Từ PT(1)(2):
\(\Rightarrow\)m(MgO+ Al2O3)(Pứ ) + mHCl(Pứ) = m(MgCl2 + AlCl3) + mH2O (theo ĐLBTKL )
\(\Rightarrow\) m(MgO + Al2O3)(Pứ) + m(MgO + Al2O3)(dư) + mHCl(pứ) = m(MgCl2+ AlCl3) + m(MgO + Al2O3)(dư) + mH2O
\(\Rightarrow\) 19,88 + 36,5a = 47,38 + 9a
\(\Rightarrow\) a = 1 (mol)
\(\Rightarrow\) nHCl(Pứ) = 1(mol)
Đổi 200ml =0,2l
\(\Rightarrow\) CM của dd HCl (đã dùng) = n : V = 1 : 0,2 = 5(M)
b) * Ta xét phần 2 :
-Vì vẫn cho t/d tiếp với dd HCl đã dùng ở thí nghiệm 1 nên CM của dd HCl dùng ở phần 2 vẫn bằng 5(M)
- Đổi 400ml = 0,4(l)
\(\Rightarrow\) nHCl = CM . V = 5 . 0,4 = 2(mol)
* Giả sử hỗn hợp chỉ có MgO
\(\Rightarrow\) nMgO = 19,88/40 = 0,497(mol)
Theo PT(2) => nHCl(tối đa cần dùng) = 2 . nMgO = 2 . 0,497 = 0,994(mol)
mà nHCl(ĐB) = 2(mol) > nHCl(tối đa cần dùng)
\(\Rightarrow\) Sau pứ : hỗn hợp hết , HCl dư
* Đặt \(\left\{{}\begin{matrix}n_{MgO}=x\left(mol\right)\\n_{Al2O3}=y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{MgO}=40x\left(g\right)\\m_{Al2O3}=102y\left(g\right)\end{matrix}\right.\)
mà mMgO + mAl2O3 = 19,88 (g)
\(\Rightarrow\) 40x + 102y = 19,88 (**)
Theo PT(1) và (2) tính ra nHCl(Pứ) = 2x + 6y (mol)
\(\Rightarrow\) mHCl (PỨ) = 36,5 . (2x + 6y ) =73 (x+ 3y)(g)
Theo PT(1)(2) tính ra nH2O = x + 3y(mol)
\(\Rightarrow\) mH2O = 18(x+ 3y)
* Theo ĐLBTKL :
m(MgO + Al2O3) + mHCl(Pứ) = m(AlCl3 + MgCl2) + mH2O
\(\Rightarrow\) 19,88 + 73.(x+3y) = 50,68 + 18(x+3y)
\(\Rightarrow\) x + 3y = 0,56 (***)
Từ (**)(***) => 40x + 102 y = 19,88 và x + 3y =0,56
\(\Rightarrow\) x=y=0,14(mol)
=> \(\left\{{}\begin{matrix}m_{MgO\left(Phan2\right)}=40x=40.0,14=5,6\left(g\right)\\m_{Al2O3\left(Phan2\right)}=102y=102.0,14=14,28\left(g\right)\end{matrix}\right.\)
vì chia làm 2 phần = nhau
\(\Rightarrow\left\{{}\begin{matrix}m_{MgO\left(hon-hop-A\right)}=5,6.2=11,2\left(g\right)\\m_{Al2O3\left(hon-hop-A\right)}=14,28.2=28,56\left(g\right)\end{matrix}\right.\)
=> mhh A = 19,88 . 2 = 39,76 (g)
=> % mMgO / A = \(\dfrac{11,2}{39,76}.100\%=28,1\%\)
=> % mAl2O3/ A = 100% - 28,1% =71,9%
Mình viết nhầm bạn nhé ở phần đổi 400ml thành 0,4l thì sau dòng đó là nHCl = 0,4 . 5 = 2(mol) không có PT2 nhé