Tính nồng độ phần trăm và nồng độ mol của dd khi cho 25g CuSO4.5H2O vào 295g nước
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CuSO_4}=\dfrac{50}{250}=0.2\left(mol\right)\)
\(n_{FeSO_4}=\dfrac{27.8}{278}=0.1\left(mol\right)\)
\(C_{M_{CuSO_4}}=C_{M_{FeSO_4}}=\dfrac{0.1}{0.1964}=0.5\left(M\right)\)
\(m_{dd_A}=50+27.8+196.4=274.2\left(g\right)\)
\(C\%_{CuSO_4}=\dfrac{0.1\cdot160}{274.2}\cdot100\%=6.47\%\)
\(C\%_{FeSO_4}=\dfrac{0.1\cdot152}{274.2}\cdot100\%=5.54\%\)
\(n_{CuSO_4.5H_2O}=\dfrac{50}{250}=0,2\left(mol\right)\)
=> \(m_{CuSO_4}=0,2.160=32\left(g\right)\)
\(m_{H_2O}=0,2.5.18=18\left(g\right)\)
\(n_{FeSO_4.7H_2O}=\dfrac{27,8}{278}=0,1\left(mol\right)\)=> \(m_{FeSO_4}=0,1.152=15,2\left(g\right)\)
\(m_{H_2O}=0,1.7.18=12,6\left(g\right)\)
\(m_{dd}=196,4+50+27,8=274,2\left(g\right)\)
\(V_{dd}=\dfrac{196,4+18+12,6}{1000}=0,227\left(l\right)\)
=> \(CM_{CuSO_4}=\dfrac{0,2}{0,227}=0,72M\)
\(C\%_{CuSO_4}=\dfrac{32}{274,2}.100=11,67\%\)
\(CM_{FeSO_4}=\dfrac{0,1}{0,227}=0,44M\)
\(C\%_{CuSO_4}=\dfrac{15,2}{274,2}.100=5,54\%\)

a) C% = 25.100/125 = 20%.
b) Nếu thêm 100ml nước thì V = 200 ml. ---> CM = nNa2SO4/0,2 = 28,4/142/0,2 = 1 M.

Câu 1 :
Khối lượng dung dịch là : \(m_{ct}+170\)
Gọi khối lượng muối \(NaNO_3\)cần dùng là x
Ta có :\(m_{ct}=\frac{C\%.m_{dd}}{100}\)
hay \(x=\frac{15.\left(x+170\right)}{100}\)
Ta tính được x=30 (g)
Vậy khối lượng \(NaNO_3\)cần lấy là 30 g

\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
=> \(C_M=\dfrac{0,2}{0,3}=0,667M\)
\(m_{dd}=300.1,05=315\left(g\right)\)
=> \(C\%=\dfrac{21,2}{315}.100\%=6,73\%\)

a) Ta có : mdd = 50 (g)
mct = 0,5 (g)
=> Nồng độ % lúc đầu của dung dịch là :
C%dd = \(\dfrac{0,5}{50}.100\%=1\%\)
Vậy lúc đầu dung dịch có nồng độ % là 1%
b)PTHH TQ : CaCl2 + H2O -> dung dịch CaCl2
Ta có : mCaCl2\(_{\left(trong-25gCaCl2.6H2O\right)}=\dfrac{111.25}{219}\approx21,67\left(g\right)\)
=> nCaCl2 = \(\dfrac{12,6}{111}\approx0,114\left(mol\right)\)
mH2O\(_{\left(trong-25gCaCl2.6H2O\right)}=25-12,67=12,33\left(g\right)\)
ta có :
1g H2O --------------------> 1ml H2O
12,33g H2O----------------> 12,33ml H2O
=> Vdd = 12,33 + 300 = 312,33 ml
mddCaCl2 (sau p/ư) = 312,33.1,08 \(\approx\) 337,32 g
=> C%ddCaCl2 = \(\dfrac{12,67}{337,32}.100\%\approx3,756\%\)
CM dd CaCl2 = \(\dfrac{n}{V}=\dfrac{0,114.1000}{312,33}\approx0,365\left(M\right)\)
Vậy........

a) nCuSO4.5H2O=0,15(mol)
-> nCuSO4=0,15(mol) -> mCuSO4=160.0,15= 24(g)
mddCuSO4(sau)= 37,5+ 162,5=200(g)
C%ddCuSO4(sau)= (24/200).100= 12%
b) mCuSO4(tách)= (200/100) x 10=20(g)

\(a)m_{dd}=4+2,8+118,2=125g\\ C_{\%NaOH}=\dfrac{4}{125}\cdot100\%=3,2\%\\ C_{\%KOH}=\dfrac{2,8}{125}\cdot100\%=2,24\%\\ b)n_{NaOH}=\dfrac{4}{40}=0,1mol\\ \\ n_{KOH}=\dfrac{2,8}{56}=0,05mol\\ 125ml=0,125l\\ C_{M_{NaOH}}=\dfrac{0,1}{0,125}=0,8M\\ C_{M_{KOH}}=\dfrac{0,05}{0,125}=0,4M\)
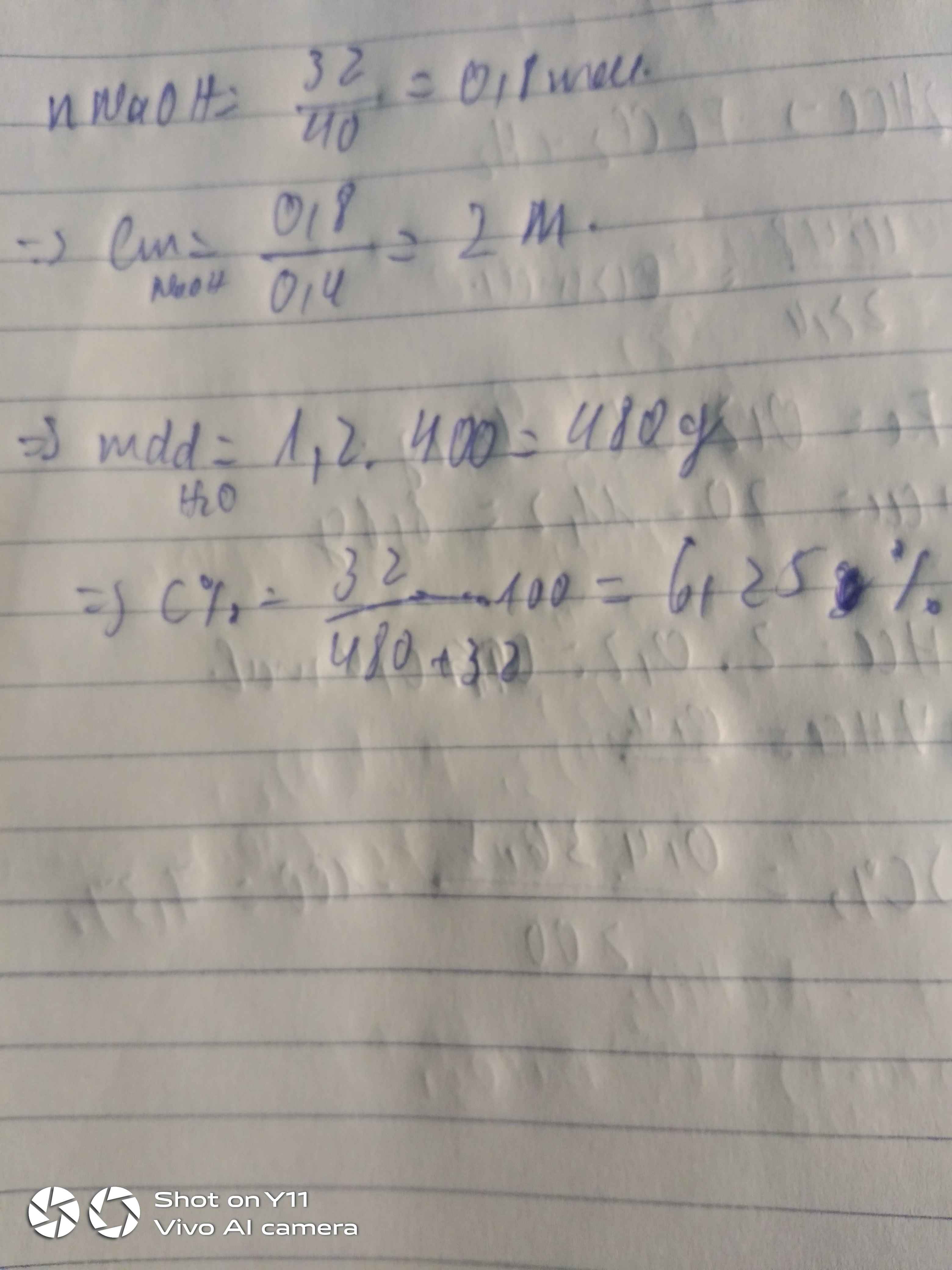
đề có sai không bạn , mình nghĩ phải là : CuSO4.5H2O chứ
khối lượng dung dịch là
mdd=mct +mdm=25+295=320(g)
nồng độ phần trăm của dung dịch là
C%=\(\dfrac{mct}{mdd}\).100%
C%dd= \(\dfrac{25}{320}\).100= 7,8 %
theo đầu bài ta có
Vdd=\(\dfrac{mdd}{Ddd}\)
Vdd=\(\dfrac{320}{1}\)=320 ml
nCuSO4.5H2=\(\dfrac{25}{170}\)= 0, 15 (mol)
nồng độ mol của dung dịch là
CM=\(\dfrac{n}{V}\)
CMdd= \(\dfrac{0,15}{0,32}\)= 0,47 M