Cần bao nhiêu gam KMnO4 để phản ứng với A dung dịch axít HCl ( đu ) thu được lượng khí Cl2 tác dụng vừa đủ với sắt tạo thành 16,25 gam FeCl3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{FeCl_3}=\dfrac{16.25}{162.5}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(......0.15......0.1\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.06...............0.48........................................0.15\)
\(m_{KMnO_4}=0.06\cdot158=9.48\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{0.48}{1}=0.48\left(l\right)=480\left(ml\right)\)
\(2Fe+ 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = \dfrac{3}{2}.\dfrac{16,25}{162,5} = 0,15(mol)\\ 2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O\\ n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,06(mol)\\ \Rightarrow m_{KMnO_4} = 0,06.158 = 9,48(gam)\\ n_{HCl} = \dfrac{16}{4}n_{Cl_2} = 0,48(mol)\\ \Rightarrow V_{dd\ HCl} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml)\)

2Fe+ 3Cl2=(t0) 2FeCl3
nFeCl3=16,25/162,5=0,1 mol => nCl2=3/2nFeCl3=3/2.0,1=0,15 mol
2KMnO4+ 16HCl=2KCl+2MnCl2+5Cl2+8H2O
nKMnO4=2/5.nCl2=2/5. 0,15=0,06 mol --> mKMnO4=0.06. 158=9,48 g
nHCl=16/5. nCl2=16/5. 0,15=0,48 mol
--> VddHCl=0,48/ 1=0,48 lit= 480 ml

\(n_P=\dfrac{12}{31}mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(\dfrac{12}{21}\)\(\rightarrow\)\(\dfrac{5}{7}\)
Khối lượng \(KMnO_4\) cần dùng để thu lượng khí trên:
\(2KMnO_4\underrightarrow{t^o}K_2MnO_2+MnO_2+O_2\)
\(\dfrac{10}{7}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(\Rightarrow m_{KMnO_4}=\dfrac{10}{7}\cdot158=225,71g\)
Nếu không dùng \(KMnO_4\) mà dùng \(KClO_3\) để thu được khí đủ dùng trên:
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{10}{21}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(m_{KClO_3}=\dfrac{10}{21}\cdot122,5=58,33g\)

2Fe + 3Cl2 --> 2FeCl3
16,25 gam FeCl3 tương đương với 0,1 mol FeCl3
Từ phương trình ta thấy để tạo ra được 0,1 mol FeCl3 thì số mol Cl2 dùng để phản ứng = 0.1.3/2 = 0,15 mol
Điều chế Clo: MnO2 + 4HCl --> MnCl2 + Cl2 + H2O
Mà để điều chế 0,15 mol Cl2 thì cần 0,15 mol MnO2 tức 0,15.87=13,05 gam MnO2 và 0,6 mol HCl => VHCl 1M = 0,6 lít

Câu 1:
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{16,25}{65}=0,25\left(mol\right)\)
\(n_{H_2}=n_{Zn}=0,25\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,25.24,79=6,1975\left(l\right)\)
c, \(n_{HCl}=2n_{Zn}=0,5\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{18,25}{10\%}=182,5\left(g\right)\)
d, \(n_{ZnCl_2}=n_{Zn}=0,25\left(mol\right)\)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{0,25.136}{16,25+182,5-0,25.2}.100\%\approx17,15\%\)
Câu 2:
a, \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
c, \(n_{NaOH}=\dfrac{40}{40}=1\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=\dfrac{1}{2}n_{NaOH}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{0,5}{2}=0,25\left(l\right)\)
d, \(n_{Na_2SO_4}=\dfrac{1}{2}n_{NaOH}=0,5\left(mol\right)\)
\(\Rightarrow C_{M_{Na_2SO_4}}=\dfrac{0,5}{0,25}=2\left(M\right)\)

\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(.........0.6............0.3\)
\(C_{M_{HCl}}=\dfrac{0.6}{0.3}=2\left(M\right)\)
\(n_{Fe_2O_3}=\dfrac{48}{160}=0.3\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{t^0}}2Fe+3H_2O\)
\(1..............3\)
\(0.3..........0.3\)
\(LTL:\dfrac{0.3}{1}>\dfrac{0.3}{3}\Rightarrow Fe_2O_3dư\)
\(n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}\cdot0.3=0.2\left(mol\right)\)
\(m_{Fe}=0.2\cdot56=11.2\left(g\right)\)

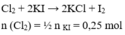
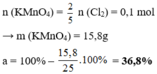

Ta có pthh 1
2KMnO4 + 16HCl \(\rightarrow\) 2KCl + 2MnCl2 + 8H2O +5Cl2
Pthh 2
3Cl2 + 2Fe \(\rightarrow\) 2FeCl3
Theo đề bài ta có
nFeCl3=\(\dfrac{16,25}{162,5}=0,1mol\)
Theo pthh 2
nCl2=\(\dfrac{3}{2}nFeCl3=\dfrac{3}{2}.0,1=0,15mol\)
Theo pthh 1
nKMnO4=\(\dfrac{2}{5}nCl2=\dfrac{2}{5}.0,15=0,06mol\)
\(\Rightarrow\) mKMnO4=0,06.158=9,48 g
Cẩm Vân Nguyễn Thị em mới làm cô xem đúng ko ạ