Cho 2,4 gam kim loại X hóa trị II vào 200 ml dung dịch HCl 0,75M thấy sau phản ứng vẫn còn một phần kim loại chưa tan hết. Cũng 2,4 gam X tác dụng với 250ml dung dịch HCl 1M thấy sau phản ứng vẫn còn axit dư. Kim loại X là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s

Đề cho thiếu chỗ nồng độ HCl (125ml)
A+2HCl==>ACl2+H2(1)
\(n_{HCl}=\frac{100}{1000}.1,5=0,15mol\)
\(n_A=\frac{2,4}{A}\)
Vì kim loại không tan hết nên: \(\frac{\frac{2,4}{A}}{1}>\frac{0,15}{2}\)
\(\frac{2,4}{A}>0,075\Rightarrow A< 32\)
A+2HCl==>ACl2+H2(2)
\(n_{HCl}=\frac{125}{1000}.2=0,25mol\)
\(n_A=\frac{2,4}{A}\)
Vì axit dư nên: \(\frac{2,4}{A}< \frac{0,25}{2}\)
=> \(\frac{2,4}{A}< 0,125\Rightarrow A>19,2\)
Vậy A là Mg ( II)

Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
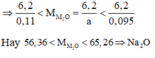
Đáp án B
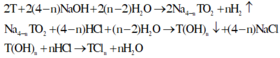
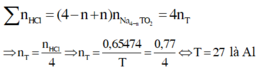
- Khi cho 2,4g X vào 200ml ddHCl 0,75M
nHCl = 0,2.0,75 = 0,15 (mol)
....\(X+2HCl\rightarrow XCl_2+H_2\)
0,075.....0,15...............................(mol)
do X còn dư nên \(\dfrac{2,4}{X}>0,075\Leftrightarrow X< 32\) (1)
- Khi cho 2,4g X vào 250ml ddHCl 1M
nHCl = 0,25.1 = 0,25 (mol)
...\(X+2HCl\rightarrow XCl_2+H_2\)
\(\dfrac{2,4}{X}\)......\(\dfrac{4,8}{X}\)..............................(mol)
axit còn dư \(\Rightarrow\dfrac{4,8}{X}< 0,25\Leftrightarrow X>19,2\) (2)
Từ (1) và (2) \(\Rightarrow\) 19,2 < X < 32 mà X là kim loại hóa trị II \(\Rightarrow X=24\)
Vậy kim loại X là Mg