72. Nung 63,9 gam Al(NO3)3 một thời gian để nguội cân lại được 31,5gam chất rắn. Tính hiệu suất của phản ứng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
Ta có hệ:
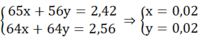
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()

Đáp án D
Theo ĐL bảo toàn khối lượng:
m O 2 = 23 , 2 - 16 , 8 = 6 , 4 ( g )
→nO = 6,4/16 = 0,4 mol
Phản ứng của HCl với chất rắn X có thể được biểu diễn với sơ đồ:
O2- + 2H+ → H2O
0,4 0,8
VHCl = 0,8 : 2 = 0,4 (lít) = 400ml

Đáp án D
Theo Đl bảo toàn khối lượng:
![]()
→ nO = 6,4/16 = 0,4 mol
Phản ứng của HCl với chất rắn X có thể được biểu diễn với sơ đồ:
O2- + 2H+ → H2O
0,4 0,8
VHCl = 0,8 : 2 = 0,4 (lít) = 400ml

Đáp án A
Sơ đồ: m(g) 0,95m (g) hh (PbO và PbS dư) + SO2
Áp dụng ĐLBTKL ta có:
mO = m - 0,95m = 0,05m (g) → nO = 3,125.10-3m (mol)
Ta có: nPbS phản ứng = nPbO = nO = 3,125.10-3m (mol)
![]()

Ta có: mO (trong oxit) = 10 - 8,4 = 1,6 (g)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Giả sử: \(n_{SO_2}=x\left(mol\right)\)
Theo ĐLBT mol e, có: 0,15.3 = 0,1.2 + 2x
⇒ x = 0,125 (mol)
\(\Rightarrow V_{SO_2}=0,125.22,4=2,8\left(l\right)\)
Bạn tham khảo nhé!

a)
$\%m_{Cu\ bị\ oxi\ hóa} = \dfrac{8}{12,8}.100\% = 62,5\%$
b)
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
$CuO + 2HCl \to CuCl_2 + H_2O$
Ta có :
$n_{CuCl_2} = n_{Cu\ pư} = \dfrac{12,8 - 8}{64} = 0,075(mol)$
$CuCl_2 + 2KOH \to Cu(OH)_2 + 2KCl$
$n_{Cu(OH)_2} = n_{CuCl_2} = 0,075(mol)$
$m_{Cu(OH)_2} = 0,075.98 = 7,35(gam)$

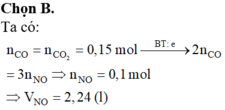
$4Al(NO_3)_3 \xrightarrow{t^o} 2Al_2O_3 + 12NO_2 + 3O_2$
Gọi $n_{O_2} = a(mol) \Rightarrow n_{NO_2} = 4a(mol)$
Bảo toàn khối lượng :
$63,9 = 31,5 + 32a + 4a.46 \Rightarrow a = 0,15(mol)$
$n_{Al(NO_3)_3} = \dfrac{4}{3}n_{O_2} = 0,2(mol)$
$H = \dfrac{0,2.213}{63,9}.100\% = 66,67\%$