cho 5,4g Al vào 400ml dung dịch CuSO4 1M, sau phản ứng hoàn toàn thu đc m gam KL và dung dịch A. Tính gía trị m và CM chất tan trog dung dịch A
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

20 tháng 8 2018
Đáp án D
H 2 NC 3 H 5 COOH 2 : 0 , 09 mol HCl : 0 , 2 mol + NaOH → H 2 NC 3 H 5 COONa 2 NaCl NaOH dư + H 2 O


10 tháng 2 2018
Đáp án A
n Fe = 0 , 12 ; n HNO 3 = 0 , 4
Tương tự như Câu 6, trong dung dịch X, gọi
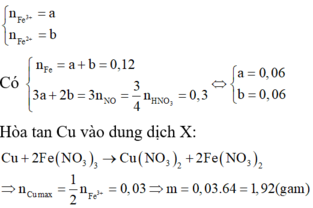
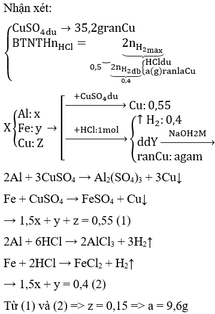
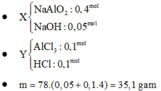

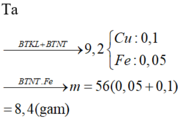


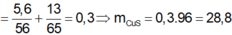
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
400ml = 0,4l
Số mol của dung dịch đồng (II) sunfat
CMCuSO4 = \(\dfrac{n}{V}\Rightarrow n=C_M.V=1.0,4=0,4\left(mol\right)\)
Pt : 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu\(|\)
2 3 1 3
0,2 0,4 0,1 0,3
Lập tỉ số so sánh : \(\dfrac{0,2}{2}< \dfrac{0,4}{3}\)
⇒ Al phản ứng hết , CuSO4 dư
⇒ Tính toán dựa vào số mol của Al
Số mol của đồng
nCu = \(\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
Khối lượng của đồng
mCu = nCu . MCu
= 0,3 .64
= 19,2 (g)
Số mol của nhôm sunfat
nAl2(SO4)3 = \(\dfrac{0,3.1}{3}=0,1\left(mol\right)\)
Nồng độ mol của nhôm sunfat
CMAl2(SO4)3 = \(\dfrac{n}{V}=\dfrac{0,1}{0,4}=0,25\left(M\right)\)
Số mol dư của dung dịch đồng (II) sunfat
ndư = nban đầu - nmol
= 0,4 - (\(\dfrac{0,2.3}{2}\))
= 0,1 (mol)
Nồng độ mol của dung dịch đồng (II) sunfat
CMCuSO4 = \(\dfrac{n}{V}=\dfrac{0,1}{0,4}=0,25\left(M\right)\)
Chúc bạn học tốt