Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P ⇒ trong 1 mol Ca3(PO4)2 có 1mol P2O5 nghĩa là trong 310g Ca3(PO4)2 tương ứng có 142g P2O5.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
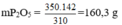
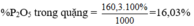

\(m_{Ca_3\left(PO_4\right)_2}=5.35\%=1,75\left(tấn\right)\)
Trong 1 mol Ca3(PO4)2 có 1 mol P2O5
=> Trong 310 tấn Ca3(PO4)2 tương ứng có 142 tấn P2O5
=> Trong 1,75 tấn Ca3(PO4)2 tương ứng có x tấn P2O5
=> x=\(\dfrac{1,75.142}{310}=0,8\left(tấn\right)\)
=> Chọn B

\(m_{Ca_3\left(PO_4\right)_2}=20\cdot40\%=8\left(tấn\right)=8000\left(kg\right)\)
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{8000}{310}=\dfrac{800}{31}\left(kmol\right)\)
Bảo toàn nguyên tố P :
\(n_{P_2O_5}=n_{Ca_3\left(PO_4\right)_2}=\dfrac{800}{31}\left(kmol\right)\)
\(m_{P_2O_5}=\dfrac{800}{31}\cdot142=3664.5\left(kg\right)\)

Đáp án B
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng P2O5 có trong loại phân đó
Lấy 100 gam quặng => mCa3(PO4)2 = 35 (g) => nCa3(PO4)2 = 0,1129 (mol)
BTNT P: => nP2O5 = nCa3(PO4)2 = 0,1129 (mol)
=> Độ dinh dưỡng =% P2O5 = [( 0,1129. 142) :100].100% = 16,03%

Để điều chế phân đạm NH4NO3 cần phải có NH3 và HNO3.
Từ không khí, than, nước, có thể lập sơ đồ điều chế phân đạm NH4NO3 như sau:
 → NO → NO2 → HNO3 → NH4NO3
→ NO → NO2 → HNO3 → NH4NO3
C + O2 → CO2: cung cấp nhiệt cho các phản ứng.
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.

Đáp án B
Giả sử khối lượng phân là 100g
⇒ mCa3(PO4)3 = 35 gam.
Bảo toàn nguyên tố ta có:
Ca3(PO4)2 → P2O5.
⇒ mP2O5 = 35 × 142/310 = 16,03 gam.
⇒ Độ dinh dưỡng của phân bón đã cho = ![]() = 16,03%.
= 16,03%.

Đáp án B
Giả sử khối lượng phân là 100g ⇒ mCa3(PO4)3 = 35 gam.
Bảo toàn nguyên tố ta có: Ca3(PO4)2 → P2O5.
⇒ mP2O5 = 35 × 142/310 = 16,03 gam.
⇒ Độ dinh dưỡng của phân bón đã cho = 16,03×100/100 = 16,03%.

Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.
Có thể tính như sau: Trong 310 gam Ca3(PO4)2(3CaO.P2O5) có chứa x gam P2O5.
Từ đó ta tính được khối lượng P2O5: x = 142 x (35 : 310) = 16 (g)
Hàm lượng P2O5 là 6%.