trong tinh thể hidrat hóa của muối sunfat kim loại có hóa trị 2, thành phần nước tinh khiết chiếm 20,93%, S chiếm 18,61%. hãy xác định công thức hóa học
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


gọi công thức của muối là A(NO3)3. nH2O , %N = 10,396
<=> ( 14*3*100)/( A + 186 + 18n) = 10,396 => A + 186 + 18n = 404 (1)
mặt khác % H2O = 40,099 => ( 18*n) /( A+ 186 +18n) = 40,009 (2)
từ 1 và 2 => n=9 , A=56 => công thức cần tìm là Fe(NO3)3.9H2O

Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
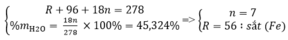
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O

CTHH: R(OH)2.xH2O
\(\%m_{OH}=100\%-24\%-60,88\%=15,12\%\)
Xét \(\dfrac{m_R}{m_{OH}}=\dfrac{60,88\%}{15,12\%}=\dfrac{761}{189}\)
=> \(\dfrac{1.M_R}{2.17}=\dfrac{761}{189}\)
=> MR = 137 (g/mol)
=> R là Ba
=> CTHH: Ba(OH)2.xH2O
Có: \(\%H_2O=\dfrac{18x}{171+18x}.100\%=24\%\)
=> x = 3
=> CTHH: Ba(OH)2.3H2O

Ta có :
\(\%H_2O = \dfrac{18n}{M + 62.3 + 18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ %N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2)\Rightarrow M = 56(Sắt) ; n = 9\)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)
\(\%H_2O= \dfrac{18n}{M + 62.3+18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ \%N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2) \Rightarrow M = 56(Sắt) ; n = 9\\ \)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)

Gọi công thức phân tử ngậm nước là: \(RSO_4.nH_2O\)
Đề bài quá mơ hồ . Phiền em xem lại đề bài rồi

CTHH: R(NO3)2.xH2O (A)
\(\%m_{NO_3^-}=100\%-42,1875\%-9,375\%=48,4375\%\)
Xét \(\dfrac{m_R}{m_{NO_3^-}}=\dfrac{1.M_R}{2.62}=\dfrac{9,375\%}{48,4375\%}\)
=> MR = 24 (g/mol)
=> R là Mg
(A) có CTHH là Mg(NO3)2.xH2O
Có: \(\%m_{H_2O}=\dfrac{18x}{148+18x}.100\%=42,1875\%\)
=> x = 6
=> CTHH: Mg(NO3)2.6H2O

Gọi CT của oxit R là RO
PTHH
RO + H2SO4 -> RSO4 + H2O (1)
nH2SO4 = 0,5 mol
Theo (1) nRO = nH2SO4 = 0,5 mol
MRO = 28/ 0,5 = 56 (g/mol)
MR = 40 (g/ mol)
R là Ca
a. CT của oxit là CaO [cái này bạn giải được rồi nên mình k giải lại]
Gọi CT của hidrat là CaSO4.nH2O
Vì số mol của hidrat = số mol của CaSO4= 0,5 mol
M CaSO4.nH2O = 86/0,5 =172 (g/mol)
136 + 18*n = 172
n = 2
CT của hidrat là CaSO4.2H2O
CTHH dạng TQ là BSO4.xH2O
* Có : %S/muối tinh thể = \(\dfrac{1.M_S}{M_{BSO4.xH2O}}.100\%=18,61\%\)
=> \(\dfrac{32}{M_{BSO4.xH2O}}=0,1861\)
=> MBSO4.xH2O =172(g)
* Có : %H2O/muối tinh thể = \(\dfrac{x.M_{H2O}}{M_{BSO4.xH2O}}.100\%=20,93\%\)
=> \(\dfrac{x.18}{172}=0,2093\)
=> x = 2
* Lại có : MBSO4.xH2O = 172(g)
mà x =2
=> MB + 96 + 2 .18 =172 => MB = 40(g) => B là Canxi(Ca)
=> CTHH là CaSO4.2H2O
cậu j ơi cậu giỏi thật đó