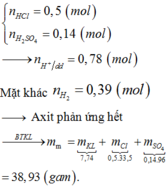Hoà tan hết hỗn hợp gồm 0,01 mol Mg và 0,02 mol Al bằng 500 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,3M, thu được dung dịch X và V lít khí H2 (đktc). Tính V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Số mol của Hiđro bằng: n H 2 = 8 , 736 22 , 4 = 0 , 39 ( m o l )
Lại có n H C l = 500 1000 . 1 = 0 , 5 ( m o l ) ; n H 2 S O 4 = 500 1000 . 0 , 28 = 0 , 14 ( m o l )
Khối lượng muối tạo thành bằng: 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 (gam).

\(n_{HCl}=0,8.0,5=0,4\left(mol\right);n_{H_2SO_4}=0,8.0,75=0,6\left(mol\right)\)
=> \(n_{Cl^-}=0,4\left(mol\right);n_{SO_4^{2-}}=0,6\left(mol\right)\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H:
\(n_{HCl}.1+n_{H_2SO_4}.2=n_{H_2}.2+n_{H_2O}.2\)
\(\Leftrightarrow0,4.1+0,6.2=0,2.2+n_{H_2O}.2\)
=>\(n_{H_2O}=0,6\left(mol\right)\)
=> \(n_O=0,6\left(mol\right)\)
\(m_{muối}=m_{kimloai}+m_{Cl^-}+m_{SO_4^{2-}}\)
=>\(m_{kimloai}=88,7-35,5.0,4-0,6.96=16,9\left(g\right)\)
=> \(m=m_{kimloai}+m_O=16,9+0,6.16=26,5\left(g\right)\)

\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
\(n_{H_2SO_4\left(bđ\right)}=1.0,5=0,5\left(mol\right)\)
Do nH2 < nH2SO4(bd) => H2SO4 dư
Gọi số mol Al, Mg là a, b (mol)
=> 27a + 24b = 9 (1)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
a--------------------------->1,5a
Mg + H2SO4 --> MgSO4 + H2
b----------------------->b
=> 1,5a + b = 0,45 (2)
(1)(2) => a = 0,2 (mol); b = 0,15 (mol)
=> mAl = 0,2.27 = 5,4 (g); mMg = 0,15.24 = 3,6 (g)