nung hỗn hợp muối gồm (CaCO3 và MgCO3) thu được 7,6 gam hỗn hợp 2 oxit và khí A . Hấp thụ khí A bằng dung dịch NaOH dư thu được 15,9 gam muối trung tính . Tính khối lượng của hỗn hợp muối
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{CO_2}=\dfrac{3,36}{22,4}.44=6,6(g)\)
Áp dụng định luật BTKL: \(m_{\text{hh muối}}=m_{\text{hh oxit}}+m_{CO_2}=76+6,6=82,6(g)\)

PTHH: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\) (1)
\(MgCO_3\xrightarrow[]{t^o}MgO+CO_2\) (2)
\(2NaOH+CO_2\xrightarrow[]{t^o}Na_2CO_3+H_2O\) (3)
\(n_{Na_2CO_3}=\dfrac{15,9}{106}=0,15\left(mol\right)\)
=> \(n_{CO_2}=0,15\left(mol\right)\)
Bảo toàn khối lượng pư 1,2:
\(m_{hh}=m_{oxit}+m_{CO_2}=7,6+0,15\times44=14,2\left(g\right)\)
vậy khối lượng hh muối là 14,2 gam

Đáp án C
Theo định luật bảo toàn khối lượng ta có:
mEste? + mNaOH? = mMuối✓ + mAncol✓
Khi đốt muối của axit no đơn chức mạch hở ta có phản ứng:
2CnH2n–1O2Na + (3n–2)O2 → t o Na2CO3 + (2n–1)CO2 + (2n–1) H2O.
⇒ nCO2 = nH2O Û mDung dịch giảm = mCaCO3 – mCO2 – mH2O.
Đặt nCO2 = nH2O = a ⇒ 100a – 44a – 18a = 3,42 Û a = 0,09 mol.
+ Từ phản ứng đốt muối ta có tỷ lệ:
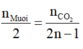 .
.
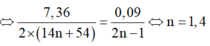
⇒ nMuối = 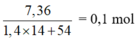 = nNaOH pứ
= nNaOH pứ
⇒ nNaOH pứ = 4 gam ✓.
+ Bảo toàn
khối lượng ⇒ mEste = 7,36 + 3,76 – 4 = 7,12 gam

Nung 26,8 gam hỗn hợp gồm CaCO3 và MgCO3, sau khi phản ứng kết thúc thu được 13,6 gam hỗn hợp gồm hai oxit và khí cacbonic.
a, Tính % khối lượng của mỗi muối trong hỗn hợp ban đầu?
b, Khí CO2 sinh ra được hấp thụ vào 200ml dung dịch Ba(OH)2 1M. Tính khối lượng muối thu được?
----
a) Gọi x,y lầ lượt là số mol CaCO3 và MgCO3 trong hh ban đầu (x,y>0)
PTHH: CaCO3 -to-> CaO + CO2
MgCO3 -to-> MgO + CO2
m(MgCO3,CaCO3)-m(2oxit)=26,8-13,6
<=> mCO2= 13,2(g) -> nCO2=0,3(mol)
Ta có hệ pt: \(\left\{{}\begin{matrix}x+y=0,3\\100x+84y=26,8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> mCaCO3=0,1.100=10(g)
\(\%mCaCO3=\frac{10}{26,8}.100\approx37,313\%\\ \rightarrow\%mMgCO3\approx62,687\%\)
b) nBa(OH)2=0,2(mol) -> nOH-=0,4(mol)
Ta có: 1< nOH-/nCO2= 0,4/0,3\(\approx1,333\) <2
-> Sp thu được hh 2 muối : BaCO3 và Ba(HCO3)2.
PTHH: Ba(OH)2 + CO2 -> BaCO3 + H2O
a______________a_________a(mol)
Ba(OH)2 + 2CO2 -> Ba(HCO3)2
b________2b________b(mol)
-> \(\left\{{}\begin{matrix}a+b=0,2\\a+2b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
=> m(muối)=mBaCO3+mBa(HCO3)2= 197.0,1+259.0,1=45,6(g)

$Na_2CO_3 + BaCl_2 \to BaCO_3 + 2NaCl$
$n_{Na_2CO_3} = n_{BaCO_3} = \dfrac{39,4}{197} = 0,2(mol)$
$n_{NaOH} = 0,2.2,5 = 0,5(mol)$
$MgCO_3 + 2HCl \to MgCl_2 + CO_2 + H_2O$
$RCO_3 + 2HCl \to RCl_2 +C O_2 + H_2O$
TH1 : NaOH dư
$2NaOH + CO_2 \to Na_2CO_3 + H_2O$
$n_{CO_2} = n_{Na_2CO_3} = 0,2(mol)$
$\Rightarrow n_{MgCO_3} = n_{RCO_3} = n_{CO_2} :2 = 0,1(mol)$
Ta có :
0,1.84 + 0,1(R + 60) = 20
=> R = 56(Fe)
Vậy :
$m_{MgCO_3} = 0,1.84 = 8,4(gam)$
$m_{FeCO_3} = 0,1.116 = 11,6(gam)$
-TH2 : có muối $NaHCO_3$
2NaOH + CO2 → Na2CO3 + H2O
0,4............0,2...........0,2........................(mol)
NaOH + CO2 → NaHCO3
0,1..........0,1.....................(mol)
$n_{CO_2} = 0,2 + 0,1 = 0,3(mol)$
$n_{MgCO_3} = n_{RCO_3} = n_{CO_2} : 2 = 0,15(mol)$
Suy ra:
0,15.84 + 0,15(R + 60) = 20
=> R = -10,6 (Loại)
Giả sử: nMgCO3 = nRCO3 = x (mol)
⇒ 84x + x(MR + 60) = 20
⇔ (MR + 144)x = 20 (1)
PT: \(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
\(RCO_3+2HCl\rightarrow RCl_2+H_2O+CO_2\)
Theo PT: \(n_{CO_2}=n_{MgCO_3}+n_{RCO_3}=2x\left(mol\right)\)
Ta có: \(n_{NaOH}=0,2.2,5=0,5\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{39,4}{197}=0,2\left(mol\right)=n_{Na_2CO_3}\)
PT: \(BaCl_2+Na_2CO_3\rightarrow BaCO_3+2NaCl\)
TH1: NaOH dư.
PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
____0,2 ________________0,2 (mol)
⇒ 2x = 0,2 ⇔ x = 0,1 (mol)
Thay vào (1), ta được MR = 56 (g/mol)
Vậy: R là Fe.
⇒ mMgCO3 = 0,1.84 = 8,4 (g)
mFeCO3 = 20 - 8,4 = 11,6 (g)
TH2: NaOH hết.
PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
____0,2____0,4________0,2 (mol)
\(CO_2+NaOH\rightarrow NaHCO_3\)
_0,1_____0,1 (mol)
⇒ nCO2 = 0,2 + 0,1 = 0,3 (mol)
⇒ 2x = 0,3 ⇔ x = 0,15 (mol)
Thay vào (1), ta được MR = -10,67 (loại)
Vậy...
Bạn tham khảo nhé!

Đáp án C
Gọi công thức chung của muối là: CnH2n+1COONa
Ta thấy đốt muối thì nCO2=nH2O
Đặt nCO2=nH2O=x=>nCaCO3=x
mdd giảm=mCaCO3-(mCO2+mH2O)
=>100x-(44x+18x)=3,42
=>x=0,09 mol
=>0,09(14n+68)=7,36(n+0,5)=>n=0,4
=>n muối=7,36(14.0,4+68)=0,1 mol
BTKL: m=m muối + m ancol – mNaOH
=7,36+3,76-0,1.40=7,12 gam
nNa2CO3=0,15 mol
MgCO3 -----> MgO+ CO2
x mol x mol x mol
CaCO3--------> CaO + CO2
y mol y mol y mol
NaOH + CO2-----> Na2CO3+ H2O
0,15mol 0,15mol
ta được hệ phương trình
\(\left\{{}\begin{matrix}56x+40y=7,6\\x+y=0,15\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
khối lượng hỗn hợp muối là
mhh=mCaCO3+mMgCO3
=100.0,05+84.0,1
=13,4g
bạn cân bằng phương trình Thứ 3 sai rồi, phải là
2NaOH + CO2 = Na2CO3 + H2O