cho 28,4(g) điphotpho penta oxit vào cốc chứa 2,7(g) H2O để tạp thành axit photphiric (H3PO4) tính khối lượng H3PO4 tạo thành
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình phản ứng:
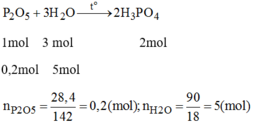
Tỉ lệ mol:
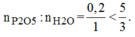
Vậy H 2 O dư và P 2 O 5 hết.
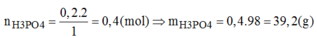
→ Chọn C.

$n_{P_2O_5} = 0,2(mol) ; n_{H_2O} = 5(mol)$
$P_2O_5 + H_2O \to 2H_3HO_4$
Ta thấy : $n_{P_2O_5} < n_{H_2O}$ nên $H_2O$ dư
$n_{H_3PO_4} = 2n_{P_2O_5} = 0,4(mol)$
$m_{H_3PO_4} = 0,4.98 = 39,2(gam)$
\(n_{P_2O_5}=\dfrac{28.4}{142}=0.2\left(mol\right)\)
\(n_{H_2O}=\dfrac{90}{18}=5\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(1.........3\)
\(0.2..........5\)
\(LTL:\dfrac{0.2}{1}< \dfrac{5}{3}\Rightarrow H_2Odư\)
\(m_{H_3PO_4}=0.2\cdot2\cdot98=39.2\left(g\right)\)

nAl = 0,5 mol
nO2 = 0,3 mol
4Al + 3O2 \(\underrightarrow{t^o}\) 2Al2O3
Đặt tỉ lệ ta có
\(\dfrac{0,5}{4}\) > \(\dfrac{0,3}{3}\)
\(\Rightarrow\) Al dư
\(\Rightarrow\) mAl dư = ( 0,5 - 0,4 ).27 = 2,7 (g)
\(\Rightarrow\) mAl2O3 = 0,2.102 = 20,4 (g)

\(1\\ 2Na + 2H_2O \to 2NaOH + H_2\\ n_{H_2} = \dfrac{1}{2}n_{Na} = \dfrac{1}{2}.\dfrac{4,6}{23} = 0,1(mol)\\ \Rightarrow V_{H_2} = 0,1.22,4 = 2,24(lít)\\ 2\\ P_2O_5 + 3H_2O \to 2H_3PO_4\\ n_{H_3PO_4} = 2.n_{P_2O_5} = 2.\dfrac{14,2}{142} = 0,2(mol)\\ \Rightarrow m_{H_3PO_4} = 0,2.98 = 19,6\ gam\)
Câu 1:
PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,1\left(mol\right)\\n_{NaOH}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\\m_{NaOH}=0,2\cdot40=8\left(g\right)\end{matrix}\right.\)
Câu 2:
PTHH: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_3PO_4}=0,2\left(mol\right)\) \(\Rightarrow m_{H_3PO_4}=0,2\cdot98=19,6\left(g\right)\)

\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{17}{32}=0,53125\left(mol\right)\\ 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\ Vì:\dfrac{0,4}{4}< \dfrac{0,53125}{5}\Rightarrow O_2dư\\ n_{O_2\left(dư\right)}=\dfrac{5}{4}.0,4=0,5\left(mol\right)\\ \Rightarrow m_{O_2\left(dư\right)}=32.\left(0,53125-0,5\right)=1\left(g\right)\\ n_{P_2O_5}=\dfrac{2}{4}.0,4=0,2\left(mol\right)\\ \Rightarrow m_{P_2O_5}=142.0,2=28,4\left(g\right)\)

\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ a,n_{P_2O_5}=n_{H_2O}:3=0,2:3=\dfrac{1}{15}\left(mol\right)\\ \Rightarrow m_{P_2O_5}=\dfrac{142.1}{15}=\dfrac{142}{15}\left(g\right)\\ b,n_{H_3PO_4}=\dfrac{2}{3}.0,2=\dfrac{2}{15}\left(mol\right)\\ \Rightarrow m_{H_3PO_4}=98.\dfrac{2}{15}=\dfrac{196}{15}\left(g\right)\)

Đáp án A
nNaOH = 0,55 mol ; nH3PO4 = 0,2 mol
=> 2 < nNaOH / nH3PO4 < 3
Các phản ứng :
2NaOH + H3PO4 -> Na2HPO4 + 2H2O
2x x
3NaOH + H3PO4 -> Na3PO4 + 3H2O
3y y
=> 2x + 3y = 0,55 ; x + y = 0,2
=> x = 0,05 ; y = 0,15 mol
=> Na2HPO4 và Na3PO4; 7,1g và 24,6g.
PTHH:P2O5+3H2O\(\underrightarrow{t^0}\)2H3PO4
Theo PTHH:142 gam P2O5 cần 54 gam H2O
Vậy:7,1 gam P2O5 cần 2,7 gam H2O
Do đó:P2O5 thừa:28,4-7,1=21,3(gam)
Vì P2O5 thừa nên ta tính SP theo chất thiếu là:H2O
Theo PTHH:54 gam H2O tạo ra 196 gam H3PO4
Vậy:2,7 gam H2O tạo ra 9,8 gam H3PO4
Vậy mH3PO4=9,8 gam
Ta có: \(n_{P_2O_5}=\frac{28,4}{142}=0,2\left(mol\right)\\ n_{H_2O}=\frac{2,7}{18}=0,15\left(mol\right)\)
PTHH: P2O5 + 3H2O -to-> 2H3PO4
Theo PTHH và đề bài, ta có:
\(\frac{0,2}{1}>\frac{0,15}{3}\)
=> P2O5 dư, H2O hết nên tính theo \(n_{H_2O}\)
Theo PTHH và đề bài, ta có:
\(n_{H_3PO_4}=\frac{2.0,15}{3}=0,1\left(mol\right)\)
Khối lượng H3PO4 tạo thành sau phản ứng:
\(m_{H_3PO_4}=0,1.98=9,8\left(g\right)\)