cho 6 lít hỗn hợp CO2,N2 ở đkc khi đi qua dung dịch KOH tạo ra 2,07 gam K2CO3 và 6gam KHCO3 . thành phần % thể tích của CO2 trong hỗn hợp là
A. 42%
B. 56%
C. 28%
D.50%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
+ n C O 2 = n K 2 C O 3 + n K H C O 3 = 0 , 075 ⇒ % n C O 2 = 0 , 075 . 22 , 4 6 = 28 %

tính theo phương trình là ra : 1) CO2 + 2KOH === > K2CO3 + H2O
2) CO2 + KOH ==== > KHCO3
N2 ko phản ứng
Đáp số 28 %

Đáp án B
Đặt n N 2 = x mol; nCO = y mol; n C O 2 = z mol
→ x+y+z=3,36/22,4= 0,15 mol
C O + C u O → t 0 C u + C O 2 ( 1 ) y y y m o l
ta có: y = nCu = 4,8/64= 0,075 mol; n C O 2 = y + z mol
CO2+ Ca(OH)2 → CaCO3+ H2O
Ta có: n C a C O 3 = n C O 2 = y+z = 10/100 = 0,1 mol →z = 0,025 mol
→x = 0,05 mol→% V N 2 = % n N 2 = 33,33%

Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol CaCO3 = 1_100=0,01 mol
Bài toán này có thể là 1 trong 2 trường hợp sau:
TH1: Số mol CO2 không đủ tác dụng với số mol Ca(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Số mol CO2 = số mol CaCO3 =0,01 mol
=>Thể tích CO2 = 22,4.0,01=0,224 lít
Vậy %thể tích CO2 = (0,224.100)/10=2,24%
TH2: Số mol CO2 nhiều hơn số mol Ca(OH)2 tham gia phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
CaCO3 + CO2 + H2O → Ca(HCO3)2 (2)
Theo (1): số mol CO2 (1) = số mol CaCO3 = Số mol Ca(OH)2 = 0,04 mol
Ta có: Số mol CaCO3 (2) = 0,04-0,01 = 0,03 (mol)
Theo (2): Số mol CO2(2) = số mol CaCO3 (2) = 0,03 (mol)
Vậy tổng số mol CO2 phản ứng (1) và (2) là 0,04 + 0,03 = 0,07 mol
Do đó %thể tích CO2 = (0,07.22,4.100)/10 = 15,68%

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

a)Gọi \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{N_2}=y\left(mol\right)\end{matrix}\right.\)
Giả sử \(n_X=1mol\Rightarrow x+y=1\left(1\right)\)
\(d_X\)/O2=1,225\(\Rightarrow\overline{M_X}=1,225\cdot32=39,2\)
\(\Rightarrow\dfrac{44x+28y}{x+y}=39,2\Rightarrow4,8x-11,2y=0\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,7\\y=0,3\end{matrix}\right.\)
\(\%V_{N_2}=\dfrac{0,3}{1}\cdot100\%=30\%\)
b)\(n_{CaCO_3}=\dfrac{20}{100}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(V=0,2\cdot22,4=4,48l\)

Đáp án : A
Muối Kali của Val và Ala có dạng: CnH2nNO2K
2 CnH2nNO2K + O2 → (2n – 1 )CO2 + 2n H2O + K2CO3 + N2
0,11 (2n – 1 ) 0,11. 2n 0,11 0,11
Đặt n H2O = x ; n CO2 = y
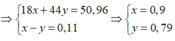
M muối = m C + m H + m (NO2K)
= 0,9.2 + 0,9. 12 + 0,11. 2 . 85
= 31,3 gam
=> m peptit = 19,88 gam
Gọi n muối của Ala = a; n muối của Val = b
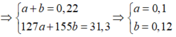
m peptit = m Ala + m Val – m H2O
= 0,1 89 + 0,12. 117 – 19,88 = 3,06 gam
=> n nước = 0, 17 mol
=> Đặt n X1 = m ; n X2 = n
∑ n H2O tách ra = 3m + 4n = 0,17 mol
∑ n gốc aminoaxit = 4m + 5n = 0,22 mol

Nếu X1 chứa p gốc Ala và X2 chứa q gốc Ala
=> 0,03. p + 0,02. q = 0,1
=> 3p + 2q = 10 => p = (10 - 3p):2 (p ≤ 4; q ≤ 5)


Đáp án D
Ta có nCa(OH)2= 2.0,02= 0,04 mol; nCaCO3= 1/100= 0,01 mol
Ta có nCa(OH)2 > nCaCO3 nên có 2 trường hợp:
- TH1: Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
Theo PT (1): nCaCO3= nCO2= 0,01 mol →VCO2=0,01.22,4=0,224 lít
→%VCO2= 2,24%→ %VN2= 100%- 2,24%=97,76%
- TH2: Ca(OH)2 phản ứng hết:
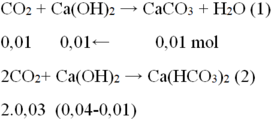
Ta có: nCO2= 0,01+ 2.0,03= 0,07 mol →VCO2= 0,07.22,4=1,568 lít
→%VCO2= 15,68%→ %VN2= 100%- 15,68%=84,32%