Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2...
Đọc tiếp
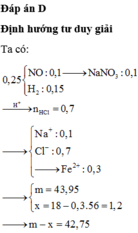
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.

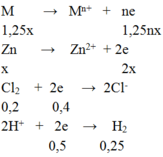
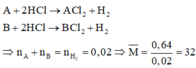



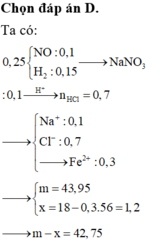
Gọi $n_{Fe} = a(mol) ; n_M = b(mol)$
$\Rightarrow 56a + Mb = 8,2 (1)$
Thí nghiệm 2 :
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$2M + nCl_2 \xrightarrow{t^o} 2MCl_n$
Theo PTHH :
$n_{Cl_2} = 1,5a + 0,5bn = 0,375(2)$
Thí nghiệm 1 :
$Fe + 2HCl \to FeCl_2 + H_2$
$2M + 2nHCl \to 2MCl_n + nH_2$
Nếu M có phản ứng với HCl :
$n_{H_2} = a + 0,5bn = 0,35(3)$
Từ (1)(2)(3) suy ra : a = 0,05 ; bn = 0,6 ; Mb = 5,4
$\Rightarrow M = \dfrac{5,4}{b} = \dfrac{5,4}{\dfrac{0,6}{n}} = 9n$
Với n = 3 thì M = 27(Al)
Nếu M không phản ứng với HCl :
$a = 0,35(4)$
Từ (1)(2)(4) suy ra a = 0,35 ; bn = -0,3 <0 (loại)
Làm sao giải đc (1), (2), (3) bằng cách nào vậy bạn