KHi hòa 3.9 g K vào 101.8 g nước, thu được KOH và khí hidro. Nồng độ % của dung dịch là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(C\%_{NaOH}=\dfrac{4}{4+2,8+118,2}.100\%=3,2\%\)
\(C\%_{KOH}=\dfrac{2,8}{4+2,8+118,2}.100\%=2,24\%\)
b, \(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,1}{0,125}=0,8\left(M\right)\)
\(n_{KOH}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(\Rightarrow C_{M_{KOH}}=\dfrac{0,05}{0,125}=0,4\left(M\right)\)

\(a,C\%_{KOH}=\dfrac{28}{140}.100\%=20\%\\ b,C\%_{KOH}=\dfrac{80}{80+320}.100\%=20\%\)

\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\\
pthh:K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
0,2 0,2 0,1
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\\
C\%_{KOH}=\dfrac{0,2.56}{200}.100\%=5,6\%\)

Câu 21 :
Pt : 2KClO3 → 2KCl + 3O2\(|\)
2 2 3
0,3 0,45
Số mol của khí oxit
nO2 = \(\dfrac{0,3.3}{2}=0,45\left(mol\right)\)
Thể tích của khí oxi ở dktc
VO2 = nO2 . 22,4
= 0,45 . 22,4
= 10,08 (g)
Câu 23 :
Số mol của kali hidroxit
nKOH = \(\dfrac{m_{KOH}}{M_{KOH}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : 500ml = 0,5l
Nồng độ mol của dung dịch thu được
CM = \(\dfrac{n}{V}=\dfrac{0,2}{0,5}=0,4\left(M\right)\)
Chúc bạn học tốt
Câu 27 :
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{1,972}{22,4}=0,08\left(mol\right)\)
Pt : Ca + H2O → Ca(OH)2 + H2\(|\)
1 1 1 1
0,08 0,08 0,08
CaO + H2O → Ca(OH)2\(|\)
1 1 1
0,04 0,04
Số mol của canxi
nCa = \(\dfrac{0,08.1}{1}=0,08\left(mol\right)\)
Khối lượng của canxi
mCa= nCa . MCa
= 0,08 . 40
= 3,2 (g)
Khối lượng của canxi oxit
mCaO = 5,44 - 3,2
= 2,24 (g)
Số mol của canxi oxit
nCaO = \(\dfrac{m_{CaO}}{M_{CaO}}=\dfrac{2,24}{56}=0,04\left(mol\right)\)
nCaO= 0,04 (mol) → nCa(OH)2 = 0,04 (mol)
Số mol tổng của canxi hidroxit
nCa(OH)2 = 0,08 + 0 ,04 = 0,12 (mol)
Khối lượng của canxi hidroxit
mCa(OH)2= nCa(OH)2. MCa(OH)2
= 0,12 . 74
= 8,88 (g)
Câu 29 :
Khối lượng của đồng (II) sunfat
C0/0CuSO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{20.70}{100}=14\left(g\right)\)
Chúc bạn học tốt

PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
Ta có: \(n_{Fe\left(OH\right)_2}=\dfrac{18}{90}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaOH}=0,4\left(mol\right)\\n_{H_2}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\\C\%_{NaOH}=\dfrac{0,4\cdot40}{160}\cdot100\%=10\%\end{matrix}\right.\)

Bài 13: nNa= 0,2 mol ; nK= 0,1 mol
2Na + 2H2O → 2NaOH + H2↑
0,2 mol 0,2 mol 0,1 mol
2K + 2H2O → 2KOH + H2↑
0,1 mol 0,1 mol 0,05 mol
a) tổng số mol khí H2 là: nH2= 0,1 + 0,05 = 0,15 mol
→VH2= 0,15 x 22,4 = 3,36 (l)
b) mNaOH= 0,2 x 40= 8 (g) ; mKOH= 0,1 x 56= 5,6 (g)
mdung dịch= mNa + mK + mH2O - mH2 = 4,6 + 3,9 + 91,5 - 0,15x2 = 99,7 (g)
→C%NaOH= 8/99,7 x100%= 8,02%
→C%KOH= 5,6/99,7 x100%= 5,62%

\(a.\)
\(m_{dd}=10+40=50\left(g\right)\)
\(C\%=\dfrac{10}{50}\cdot100\%=20\%\)
\(b.\)
\(m_{KOH}=0.25\cdot56=14\left(g\right)\)
\(m_{dd_{KOH}}=14+36=50\left(g\right)\)
\(C\%_{KOH}=\dfrac{14}{50}\cdot100\%=28\%\)

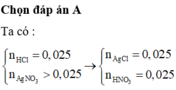
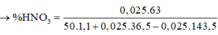
$2K + 2H_2O \to 2KOH + H_2$
$n_{KOH} = n_K = \dfrac{3,9}{39} = 0,1(mol)$
$n_{H_2} = \dfrac{1}{2}n_K = 0,05(mol)$
$m_{dd\ sau\ pư} = 3,9 + 101,8 - 0,05.2 = 105,6(gam)$
$C\%_{KOH} = \dfrac{0,1.56}{105,6}.100\% = 5,303\%$
\(n_K=0,1\left(mol\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
0,1 ----- 0,1 ------ 0,1 ----- 0,05 (mol)
\(m_{dd}\left(saupứ\right)=3,9+101,8-0,05.2=105,6\left(g\right)\)
\(\Rightarrow C\%\left(KOH\right)=\dfrac{0,1.56}{105,6}.100\%=5,3\%\)