Giúp mih câu này ạ hoá lớp 7 bài 7 tính theo công thức hoá học và phương trình hoá học theo chương trình mới khtn trang 56
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
Coi n gluxit = 1(mol)
Bảo toàn nguyên tố với C,H .Ta có :
n CO2 = n(mol)
n H2O = m(mol)
Suy ra :
18m/44n= 33/88
<=> m/n = 11/12
Với m = 11 ; n = 12 thì thỏa mãn
Vật CT của gluxit là C12(H2O)11 hay C12H22O11
Câu 2 :
a)
\((1) C_6H_{12}O_6 \xrightarrow{t^o,xt} 2CO_2 + 2C_2H_5OH\\ (2) C_2H_5OH + O_2 \xrightarrow{men\ giấm} CH_3COOH + H_2O\\ (3) CH_3COOH + C_2H_5OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O\\ (5)CH_3COO_2H_5 + NaOH \to CH_3COONa + C_2H_5OH\\ (6) 2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2\)
b)
\((1)C_{12}H_{22}O_{11} + H_2O \xrightarrow{t^o,H^+} C_6H_{12}O_6 + C_6H_{12}O_6\\ (2)C_6H_{12}O_6 \xrightarrow{t^o,xt} 2CO_2 + 2C_2H_5OH\\ (3)C_2H_5OH + CH_3COOH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O\\ (4)CH_3COOC_2H_5 + NaOH \to CH_3COONa + C_2H_5OH\)

8) PTK của \(Cu\left(NO_3\right)_x=188\) đvC
\(\Leftrightarrow64+\left(14+3.16\right).x=188\)
\(\Leftrightarrow x=2\)
9) PTK của \(K_xPO_4=203\) đvC
\(\Leftrightarrow39.x+31+4.16=203\)
\(\Leftrightarrow x=...\)
-> Xem lại đề bài câu này, 212 mới đúng
10) PTK của \(Al\left(NO_3\right)_x=213\) đvC
\(\Leftrightarrow27+\left(14+3.16\right).x=213\)
\(\Leftrightarrow x=3\)

Áp dụng nguyên tắc bảo toàn đối với nguyên tố oxi => trong X không có oxi. Vậy X là hiđrocacbon, có công thức phân tử C n H m . Từ phương trình hoá học của phản ứng cháy, ta có :
=> an = 2; am = 4
Nếu a = 1 thì n = 2; m = 4 → C 2 H 4 (phù hợp)
Nếu a = 2 thì n = 1; m = 2 → CH 2 ( không phù hợp)
Vậy công thức phân tử của X là C 2 H 4

Dạng axit - bazơ của nhôm hiđrôxit:
Al(OH)3 -→ HAlO2.H2O
Dạng Bazơ - Dạng axit( Axit aluminic )
PTHH: Al(OH)3 + NaOH → NaAlO2 + 2H2O
Axit - Bazơ
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Bazơ - Axit

4) \(M_{NH_3}=8,5.2=17\) g/mol
mN = 17.82,35% = 14 (g)
mH = 17 - 14 = 3 (g)
\(n_N=\dfrac{14}{14}=1\left(mol\right)\)
\(n_H=\dfrac{3}{1}=3\left(mol\right)\)
=> Trong 1 mol phân tử có 1 mol nguyên tử N và 3 mol nguyên tử H
=> \(NH_3\)
Câu 4 :
Ta có : MX = \(M_{H_2}.8.5=17\) (g/mol)
Có N chiếm 82.35% , H chiếm 17.65%
Nên khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là
mN = \(\dfrac{17.82,35}{100}=13.995\left(g\right)\)
=> mH = mX - mN = 3.005 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là
nN = \(\dfrac{13.995}{23}\approx0.6\left(mol\right)\)
nH = \(\dfrac{3.005}{1}\approx3\left(mol\right)\)
=> CTHH của hợp chất X là NH3
Câu 5:
a) MX = 2.207 x 29 = 64.003 \(\approx64\left(đvC\right)\)
b) Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là
mS = \(\dfrac{64.50}{100}=32\left(g\right)\)
mO = 64 - 32 = 32 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là
nS = \(\dfrac{32}{32}=1\left(mol\right)\)
nO = \(\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH của hợp chất X là \(SO_2\)

Câu 9:
\(a,K,Na_2O,SO_3\\ b,K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\\ Na_2O+H_2O\rightarrow2NaOH\\ SO_3+H_2O\rightarrow H_2SO_4\)
Câu 10:
Mg(OH)2 - bazo - magie hidroxit
NaCl - muối - natri clorua
H2SO4 - axit - axit sunfuric
Ca(HCO3)2 - muối - canxi hidrocacbonat
Câu 11:
- Khí oxi là đơn chất
- Vì trong nước có cả khí oxi
- Dùng trong lĩnh vực y học, ...
Câu 12:
\(a,n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2--------------------------->0,2
b, VH2 = 0,2.22,4 = 4,48 (l)
c, PTHH: \(2H_2+O_2\xrightarrow[]{t^o}2H_2O\)
0,2-->0,1
=> Vkk = 0,1.22,4.5 = 11,2 (l)
9
a) K , Na2O , SO3 là những chất td với H2O
b)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\\
Na_2O+H_2O\rightarrow2NaOH\\
SO_3+H_2O\rightarrow H_2SO_4\)
10
Mg(OH)2 -Magie hidroxit - bazo
NaCl - natri clorua - muối
H2SO4 - axit sunfuric - axit
Ca(HCO3)2 - canxi hidrocacbonat - muối
11
a)đơn chất
b) vì trong nước có chứa nguyên tử Oxi
c) Thợ lặn
12
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\
pthh:2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,2 0,1
\(V_{KK}=\left(0,1.22,4\right).5=11,2\left(l\right)\)


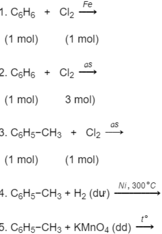
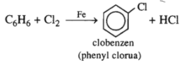
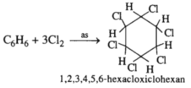
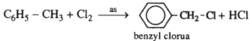
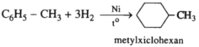
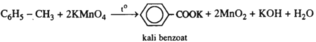
a)
Gọi hợp chất đó là A
dh/chất/H2 = 81 =) MA = 81 x 2 = 162 (g/mol)
CTHH : CxHyNz
Khối lượng của mỗi nguyên tố có trong 1 mol khí A là :
mC = \(\frac{162\times74,07\%}{100\%}=119,9934\approx120\)
mN = \(\frac{162\times17,28\%}{100\%}=27,9936\approx28\)
mH = \(\frac{162\times8,64\%}{100\%}=13,9968\approx14\)
Số mol nguyên tử của mỗi nguyên tố trong 1mol khí A là
\(n_H=\frac{m}{M}=\frac{14}{1}=14\left(mol\right)\)
\(n_C=\frac{m}{M}=\frac{120}{12}=10\left(mol\right)\)
\(n_N=\frac{m}{M}=\frac{28}{14}=2\left(mol\right)\)
=) Trong 1 mol phân tử hợp chất A có : 14 nguyên tử H , 10 nguyên tử C và 2 nguyên tử N
CTHH là : \(C_{10}H_{14}N_2\)
b) Bạn tự làm nha =)))
Chúc bạn học tốt