pu của fe du vs o,04 hno3 loãng thấy xuất hiện khi No tính m thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) $n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$Fe^0 \to Fe^{+3} + 3e$
$N^{+5} + 3e \to N^{+2}$
Bảo toàn electron : $3n_{Fe} = 3n_{NO}$
$\Rightarrow n_{NO} = 0,2(mol)$
$\Rightarrow V = 0,2.22,4 = 4,48(lít)$
b) $n_{Fe(NO_3)_3} = n_{Fe} = 0,2(mol)$
$\Rightarrow m = 0,2.242 = 48,4(gam)$

\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\\ n_{Fe}=\dfrac{6,72}{56}=0,12\left(mol\right)=n_{NO}\\V= V_{NO\left(đktc\right)}=0,12.22,4=2,688\left(l\right)=2668\left(ml\right)\)

Theo gt ta có: $n_{NO}=0,3(mol)$
Gọi số mol của Al và Fe trong 11g hỗn hợp lần lượt là a;b(mol)
Ta có: \(\left\{{}\begin{matrix}27a+56b=11\\3a+3b=0,9\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
Suy ra $m_{Fe}=5,4(g);m_{Al}=5,6(g)$
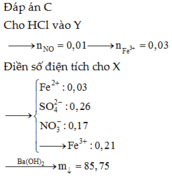
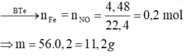
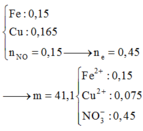

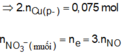
mk muốn hồi fe tác dụng vs h2so4 dn cho ra j viết pthh