Một hợp chất của nguyên tố y hoá trị III kết hợp với nguyên tố oxy hoá trị II chiếm 52,9 % theo khối lượng. a, hãy xác định Nguyên tử khối và tên nguyên tố. b, viết công thức hoá học và tính phản tử khối của hợp chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTHH của hợp chất là TxOy
Theo quy tắc hóa trị ta có :
III.x=II.y \(\Rightarrow\frac{x}{y}=\frac{II}{III}=\frac{2}{3}\)
Vậy CTHH của hợp chất là T2O3
Ta có : T chiếm 53% nên O chiếm 47%
Ta lại có:
\(x:y=\frac{\text{%T}}{M_T}:\frac{\%O}{M_O}=\frac{53}{M_T}:\frac{47}{16}\)
\(\Leftrightarrow\frac{2}{3}=\frac{53}{M_T}:\frac{47}{16}=\frac{53}{M_T}.\frac{16}{47}\)
\(\Rightarrow M_T=\frac{3.53.16}{2.47}\approx27\)
Vậy T là nhôm. KHHH : Al
\(\Rightarrow\) CTHH của hợp chất là Al2O3
Phân tử khối của Al2O3 = 27.2+16.3 = 102(đvC)

Gọi công thức của hợp chất là T 2 O 3 và a là nguyên tử khối của T.
Theo đề bài, ta có tỉ lệ phần trăm khối lượng của T:
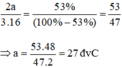
Nguyên tố T là nhôm.

Nguyên tố R tạo thành hợp chất khí với hiđro có công thức là RH 4 sẽ tạo thành hợp chất oxit cao nhất là RO 2 có phần trăm khối lượng của nguyên tô R :
100% - 72,73% = 27,27%
72,73% phân tử khối của RO 2 ứng với 16 x 2 = 32 (đvC).
27,27% phân tử khối của RO 2 ứng với nguyên tử khối của nguyên tố R là :
32x27,27/72,73 = 12 (đvC) => R là cacbon (C)

Mình gộp chung câu a và b để tính đó
Gọi CTHH của hợp chất là TxOy, theo quy tắc hóa trị ta có:
III*x=II*y→x/y=2/3→x=2, y=3
Vậy CTHH của hợp chất lầ T2O3
NTK của hợp chất là: \(\frac{16.3.100\%}{\left(100\%-53\%\right)}=102\)
NTK của T là :\(\frac{102-16.3}{2}=27\)
Vậy T là n tố Al

Gọi CTHH là Z2O5
% O = 16.5 / ( MZ.2+16.5)= 56,34%
<=> MZ ∼ 31 đvc
=> Z là photpho (P)
=> CTHH là P2O5
M P2O5 = 31.2+16.5=142 đvc

CT: Ca(XOy)
\(\frac{40+X}{16y}=\frac{52,94}{47,06}\)=> 1882,4+ 47,06X = 847,04y (chia 2 vế cho 47,06)
=> 18y = 40 + X => X= 18y-40
M= 136= 40+ X + 16y= 40+ 18y - 40 +16y
=> 34y= 136=> y= 4
X= 18y-40= 18.4 - 40= 32 ( S )
Vậy CTHH: CaSO4
sai rồi nha bạn mình có đáp án rồi
gọi CTHH của hợp chất là Y2O3 và x là nguyên tử khối của Y
theo đề ra ta có
2*x/3*16=52.9%/49%
suy ra x=27 đvc
là nguyên tố nhôm
Ta có :
a) Nguyên tử khối của Oxi là 16 đvC
Do nguyên tố Oxi chiếm 52,9% theo khối lượng
=>nguyên tố Y chiếm 47,1%
=> Tỉ lệ khối lượng của nguyên tố Y so với nguyên tố Oxi trong hợp chất là :
47,1 : 52,9 = 471 : 529
=> Nguyên tử khối của nguyên tố Y là :
16 * ( 471 : 529 ) = 14 (đvC)
=> Y là nguyên tố Nitơ ( N )
b) Gọi công thức hóa học của hợp chất là NxOy ( x,y là chỉ số của N,O)
Ta có :
Hóa trị của N * x = Hóa trị của O * y
=> III * x = II * y
=> x : y = II : III
=> x =2 ; y=3
Vậy công thức hóa học của hợp chất đó là N2O3