nhung 1 thanh sat nang 100 g vao 100 ml dd Cu(N03)2 0.2M va AgNO3 0.2M. Sau thời gian cân lại thanh sát năng 101.72g.tính khối lượng Fe phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích: Đáp án C
nCu2+ = nCu(NO3)2 = 0,2 mol
Fe + Cu2+ -> Fe2+ + Cu
1 mol Fe phản ứng tạo 1 mol Cu => mtăng = 64 – 56 = 8g
=> nFe pứ = (101,2 – 100)/8 = 0,15 mol
=> mFe pứ = 8,4g

\(\left\{{}\begin{matrix}n_{Cu\left(NO_3\right)_2}=0,2.0,1=0,02\left(mol\right)\\n_{AgNO_3}=0,2.0,1=0,02\left(mol\right)\end{matrix}\right.\)
PTHH: Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
0,01<---0,02--------->0,01---->0,02
Fe + Cu(NO3)2 --> Fe(NO3)2 + Cu
a<--------a------------->a----->a
=> 100 - 56(0,01+a) + 0,02.108 + 64a = 101,72
=> a = 0,015
=> nFe = 0,015 + 0,01 = 0,025 (mol)
=> mFe = 0,025.56 = 1,4(g)

Đáp án C
Ta cớ pứ: Fe + Cu2+ → Fe2+ + Cu.
Đặt nFepứ = a ⇒ nCu = a.
⇒ mCu – mFe pứ = 0,4 Û 8a = 0,8 Û a = 0,05.
⇒ mFeSO4 = 0,05×152 = 7,6 gam

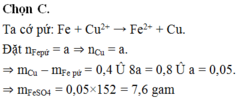
dd có:
0,02 mol Cu2+
0,02 mol Ag+
sắt dư so với Ag nên trong dd không có Fe3+
Fe + 2Ag+ ==> Fe2+ + 2Ag
0,01 0,02 0,01 0,02
nếu phản ứng này xảy ra tới hết lượng ag trong dung dịch thì khối lượng thanh kim loại là
100 - 0,01.56 + 0,02.108 = 101,6 gam < 101,72 (1)( nhỏ hơn 0,12 gam)
vì cu = 64 và ag = 108 nên sắt phản ứng càng nhiều thì khối lượng thanh sắt tăng càng nhiều
(1) chứng tỏ xảy ra tiếp phản ứng
Fe + Cu2+ ==> Fe2+ + Cu
nếu 1 mol sắt phản ứng thì sẽ klượng thanh kim loại sẽ tăng: 64 - 46 = 8 gam
vậy nhỏ hơn 0,12 gam thì sẽ có 0,015 mol Fe tham gia phản ứng này.
Vậy cộng vào, tổng mol Fe phản ứng là 0,025 mol
suy ra khối lượng fe đã phản ứng là 1,4 gam