Có 2 kim loại X và Y. Tổng số hạt trong cả 2 nguyên tử X và Y là 122. Nguyên tử Y có số nơron nhiều hơn nguyên tử X là 16 hạt và số p trong X chỉ bằng 1/2 số p trong Y. Nguyên tử khối của X bé hơn Y là 29. Xác định 2 kim loại trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi số hạt proton là P với P=E=Z
Số notron là N
Khi đó áp dụng với kl X và Y là
N1, Z1; N2, Z2
Vì tổng số hạt hai nguyên tử X và Y là 122 nên ta có
N1 + N2 + Z1 + Z2 =122 (1)
Nguyên tử Y có số notron nhiều hơn nguyên tử X là 16 hạt và số P trong X chỉ bằng 1/2 số P trong Y
N2 - N1 = 16 (2)
2(Z1) = Z2 (3)
Mặt khác nguyên tử khối của X bé hơn Y là 29
N2 - N1 + Z2 - Z1 = 29 (4)
Từ (2) và (4) ta có Z2 - Z1 = 13 kết hợp với (3) ta được Z1 = 13 và Z2 = 26
Thay Z1 và Z2 vừa tìm được vào (1) và kết hợp với (2) được N1 = 14 và N2 = 30
Vậy X là Al còn Y là Fe

Ta có
Số proton là : p = e = z
Số neutron là n
Gọi số p, n và e ở X là z1 ; n1; e1
Tương tự như vậy vs Y ta có z2 ; n2 ;e2
Ta có:
2z1 + n1 + 2z2 + n2 = 122 (1)
Y có số n nhiều hơn X là 16 => n2 - n1 = 16 (2)
Số p ở X = 1/2 số p ở Y => 2z1 = z2 (3)
Mà số khối của X bé hơn Y là 29 => n2 - n1 + z2 - z1 =29 (4)
Thế (2) vào (4) => 16 + z2 - z1 = 29 <=> z2 - z1 = 13 . Sau đó thế tiếp vào (3) , ta có:
z1 = 13; z2 = 26
Thế z1 ; z2 vào (1) ta có:
78 + n1 + n2 = 122 <=> n1 + n2 = 44
và kết hợp với (2), áp dụng tìm 2 số khi biết tổng và hiệu, ta có:
n1 = 14; n2 = 30
Vậy X là Al ; Y là Fe
Thử lại xem KQ có khớp vs các dữ liệu của đề bài ko nha.

Gọi tổng số hạt proton , electron , notron của 2 nguyên tử X và Y là M
gọi số proton , electron , notron của M lần lượt là p ,e ,n . TA CÓ :
p+e+n = 76 => 2p + n = 76 ( vì nguyên tử trung hòa về điện) (1)
do tổng số hạt mang điện tích lớn hơn tổng số hạt không mang điện tích là 24 hạt
=> 2p - n = 24
Kết hợp (1) ta được 2p = 50 => tổng số hạt mang điện tích của 2 nguyên tử X và Y là 50 hạt (*)
Từ đề ra ta lại có :
số hạt mang điện(Y) - số hạt mang điện(X) = 18(**)
Từ (*) và (**) => số hạt mang điện của Y = 34 (hạt) => Y có 17 proton => Y là nguyên tố Clo
=> số hạt mang điện của X = 16 (hạt) => X có 8 proton => X là nguyên tố Oxi

Kí hiệu : P X , P Y và N X , N Y lần lượt là số proton và số nơtron của nguyên tử X và Y.
Theo đề bài ta lập được hệ phương trình đại số :
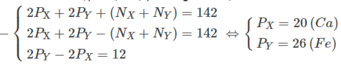

Ta có các PT
+) 2pX + 2pY + nX + nY = 80
+) (2pX + 2pY) - (nX + nY) = 24
+) 2pY - 2pX = 16
=> \(\left\{{}\begin{matrix}p_X=9\\p_Y=17\end{matrix}\right.\)
=> X là F, Y là Cl

Theo bài ra, ta có:
\(\left\{{}\begin{matrix}\dfrac{n_X}{p_X+e_X}.100\%=53,152\%\\p_X+e_X+n_X=49\\p_X=e_X\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p_X=e_X=16\\n_X=17\end{matrix}\right.\)
=> X: Lưu huỳnh (S)
Lại có: \(\left\{{}\begin{matrix}p_Y+e_Y+n_Y=52\\p_Y=e_Y\\p_Y+e_Y-n_Y=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p_Y=e_Y=17\\n_Y=18\end{matrix}\right.\)
=> Y: Clo (Cl)

Gọi p1;n1 là số proton và nơtron của ntử X; p2,n2 là số proton và notron trong ntử Y.
Ta có: 2p1+ 2p2+n1+n2=122 (3)
n2-n1=16→n2=n1+16(1) và p1=p2/2→2p1=p2(2)
Thế (1), (2) vào (3) ta được:
6p1+2n1+16=122→3p1+n1=53
mặt khác p2+n2-(p1+n1)=29(4)(vì nguyên tử khối X = số khối A1=p1+n1; nguyên tử khối Y=số khối A2=p2+n2)
Thế (1), (2) vào (4) ta được: p1=13→p2=26