Cho dung dịch A là một hỗn hợp: H2SO4 2.10-4M và HCl 6.10-4M Cho dung dịch B là một hỗn hợp: NaOH 3.10-4M và Ca(OH)2 3,5.10-4M
a) Tính pH của dung dịch A và dung dịch B
b) Trộn 300ml dung dịch A với 200ml dung dịch B được dung dịch C. Tính pH của dung dịch C.


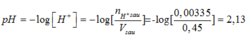
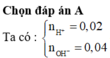
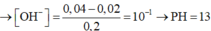
a. [ H+] trong A: 2.2.10-4 + 6.10-4 = 10-3 mol pH = 3
[OH-] trong B: 3.10-4 + 2.3,5.10-4 = 10-3 mol pOH = 3 ® pH =11
b. Trong 300ml dung dịch A có số mol H+ = 0,3.10-3 mol Trong 200 ml dung dịch B có số mol OH- = 0,2.10-3 mol
Dung dịch C có: V = 0,5 lít; số mol H+ = 0,3.10-3 - 0,2.10-3 = 10-4 mol
Dạng 2: Pha trộn dung dịch
Phương pháp giải
+ Sử dụng phương pháp đường chéo, ghi nhớ: Nước có C% hoặc CM =0.
+ Xác định số mol chất, pH ® [H+]® mol H+ hoặc mol OH-.
+ Việc thêm, cô cạn nước làm thay đổi nồng độ mol/l và không làm thay đổi số mol chất
® tính toán theo số mol chất.
Võ Đông Anh Tuấn cái R đóng khung là j z