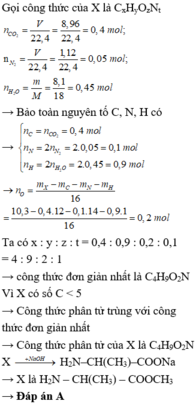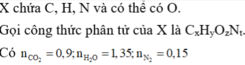Đốt cháy 0,528 gam hợp chất X thu được 1,055 gam CO2 và 0,432 gam H2O. Tìm công thức của X. Biết trong phân tử có 4 nguyên tử cacbon.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nCO2 = 0,024 mol
nC = 0,024 mol
mC = 0,288 g
nH2O = 0,024 mol
nH = 0,048 mol
mO = 0,528 - 0,288 - 0,048 = 0,192 g
nO = 0,012 mol
Gọi: CTHH là : CxHyOz
x : y : z = 0,024 : 0,048 : 0,012 = 2 : 4 : 1
CTTQ : (C2H4O)n
Vì: phân tử có 4 nguyên tử C
= n=2
Vậy: CTHH : C4H8O2

Phân huỷ 0,445 gam X thu được 0,0025 mol N2O
→ Phân huỷ 0,356 gam X thu được 0,002 mol N2O
→ Số mol N trong X: 0,004 mol → mN = 0,004.14 = 0,056 gam
nCO2 = 0,012 mol → số mol C trong X: 0,012 mol → mC = 0,144 gam
nH2O = 0,014 mol → số mol H trong X : 0,028 mol → mH = 0,028 gam
mC + mH + mN = 0,228 gam < mX = 0,356 gam
→ Trong X còn có nguyên tử oxi, mO = 0,356 - 0,228 = 0,128 mol
→ Số mol O trong X : 0,008 mol
Đặt CTHH của X là CxHyOzNt
x : y : z : t = nC : nH : nO : nN = 0,012 : 0,028 : 0,008 : 0,004 = 3 : 7 : 2 : 1
Công thức phân tử đơn giản nhất của X là C3H7O2N
Vì X chỉ chứa 1 phân tử N → CTPT trùng với công thức đơn giản nhất
→ CTPT là C3H7O2N

theo định luật bảo toàn khối lương ta có :
mA + mO2 = mCO2 + mH2O
<=> 16 + 64 = mCO2 +H2O
<=> 80 = mCO2 +H2O
đặt 9x là mH2O => mCO2 =11x
ta có : 9x+ 11x= 80
giải tìm x= 4
=>mH2O= 36 g
=>mCO2= 44

Vì sản phẩm cháy gồm Na2CO3, CO2 và H2O nên trong A chắc chắn có C, H, Na, có thể có O.
Ta có:
![]()
Vì trong A chỉ có một nguyên tử Na => nA = 0,05 mol
![]()
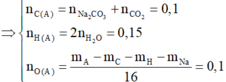
Gọi công thức phân tử của A là C x H y O z Na
Đáp án A.

Ta có : $n_{CO_2} = \dfrac{4,4}{44} = 0,1(mol) ; n_{H_2O} = \dfrac{1,8}{18} = 0,1(mol)$
Bảo toàn nguyên tố C,H :
$n_C = n_{CO_2} = 0,1(mol) ; n_H = 2n_{H_2O} = 0,2(mol)$
$\Rightarrow n_O = \dfrac{2,2 - 0,1.12 - 0,2.1}{16} = 0,05(mol)$
Ta có :
$n_C : n_H : n_O = 0,1 : 0,2 : 0,05 = 2 : 4 : 1$
Vậy CTPT của X là $C_2H_4O$