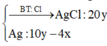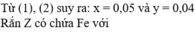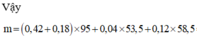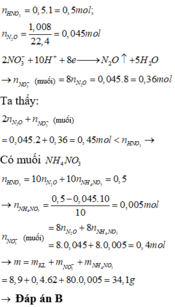cho m gam Mg vào dd HNO3 dư, sau khi phản ứng kết thúc thu được 0,1792 lít khí N2 (đktc) và dung dịch x chứa 6,67m gam muối. Tính m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn A.
Hỗn hợp X gồm Mg (4x mol) và Fe (3x mol) và dung dịch chứa FeCl3 (6y mol) và CuCl2 (y mol)
Dung dịch Y chứa Fe2+, Mg2+ (4x mol) và Cl- (20y mol)


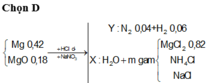
Đáp án D
n H 2 = 0 , 5 mol
Cu là kim loại đứng sau hidro trong dãy hoạt động hoá học, do đó Cu không tác dụng với dung dịch HCl
Sơ đồ phản ứng:
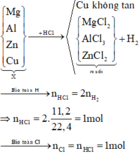
Khối lượng muối chính là khối lượng kim loại Mg, Al, Zn và Cl. Khi đó ta có:
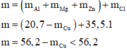
Chỉ có 49,80 < 56,2. Vậy giá trị của m có thể là 49,80 gam

Đáp án A
Số mol N2O = 1,008/22,4 = 0,045 mol;
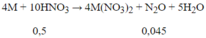
Số mol HNO3 phản ứng = 0,045.10 = 0,45 mol < 0,5 suy ra có tạo sản phẩm khử khác là NH4NO3
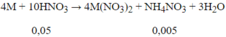
Vậy m = 8,9 + 62.( 8.0,045+8.0,005)+ 80.0.005=34,1g

Gọi n Mg = a; n Zn = b ⇒ 24a + 27b = 8,9g (1)
nHNO3 ban đầu = 0,5
nN2O = 0,045
Gọi số mol muối NH4NO3 là x mol
Bảo toàn e ta có: 2nMg + 2nZn = 8nN2O + 8nNH4NO3
⇒ 2a + 2b – 8x = 0,36 (2)
Bảo toàn nguyên tố N ta có:
n HNO3 = n NO3- trong muối KL + 2n NH4NO3 + 2n N2O
⇒10n N2O + 10n NH4NO3 = 0,5 mol ( n NO3- trong muối KL = n e = 8n NH4NO3 + 8n N2O)
⇒ n NH4NO3 = 0,005 (mol)
⇒ n NO3- trong muối KL = 0,4 mol
mmuối = mNO3-/muối KL + mKL + mNH4NO3 = 0,4.62 + 8,9 + 0,005.80 = 34,1
Đáp án B.