Một dung dịch có hoà tan hai muối là NaBr và NaCl. Nồng độ % của mỗi muối trong dung dịch đều bằng nhau và bằng C%. Hãy tính nồng độ % của hai muối trong dung dịch, biết rằng 50g dd hai muối trên tác dụng vừa đủ với 50ml dd AgNO3 8%, có khối lượng riêng D=1,0625g ml.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


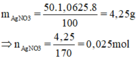
Phương trình hóa học của phản ứng:
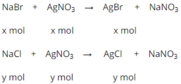
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số: 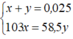
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
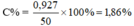

=
= 0, 025 mol
Phương trình hóa học của phản ứng:
NaBr + AgNO3 → AgBr↓ + NaNO3
X mol x mol x mol
NaCl + AgNO3 → AgCl↓ + NaNO3
Y mol y mol y mol
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Ta có hệ phương trình đại số:
Giải ra , ta có x = 0, 009 mol NaBr
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
C% = x 100% = 1,86%

Chọn đáp án A
m d d A g N O 3 = V.D = 50.1,0625 = 53,125 (gam)
ð m A g N O 3 = 53 , 125 . 8 100 = 4,25 (gam) => n A g N O 3 = 4 , 25 170 = 0,025 (mol)
Nồng độ % của 2 muối bằng nhau => Khối lượng 2 muối bằng nhau.
N a C l : x m o l N a B r : y m o l → x + y = 0 , 025 58 , 5 x = 103 y → x = 0 , 0159 y = 0 , 0091
ð
C
%
N
a
C
l
=
0
,
0159.58
,
5
50
.100% = 1,86%

ọi nồng độ muối trong dung dịch I là x (%)(x > 20), nồng độ muối trong dung dịch II là x – 20(%)
Lượng muối có trong dung dịch I là 200.x%,
lượng muối có trong dung dịch II là 300.(x -20)%.
Theo định luật bảo toàn khối lượng ta có khối lượng dung dịch tạo thành là 200 + 300 = 500g
Theo bài ra ta có phương trình:
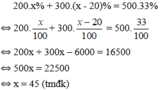
Vậy nồng độ mưới của dung dịch I là 45%, nồng độ muối của dung dịch II là 25%

Ta có: \(m_{dd}=m_{dd1}+m_{dd2}=220kg\)
Mặt khác: \(C\%_1=C\%_2+1\Leftrightarrow\frac{m_1}{m_{dd1}}.100=\frac{m_2}{m_{dd2}}.100+1\Leftrightarrow\frac{5}{m_{dd1}}.100=\frac{4,8}{m_{dd2}}.100+1\)
\(\Leftrightarrow\frac{5}{220-m_{dd2}}.100=\frac{4,8}{m_{dd2}}.100+1\)\(\Leftrightarrow m_{dd2}=120kg\)\(\Rightarrow m_{dd1}=100kg\)
Nói chung cách làm là như vậy á, co gì kiểm tra lại giúp nha

a)
Gọi $n_{NaCl} = a(mol) ; n_{KCl} = b(mol)$
$\Rightarrow 58,5a + 74,5b = 13,3(1)$
$NaCl + AgNO_3 \to AgCl + NaNO_3$
$KCl + AgNO_3 \to AgCl + KNO_3$
$n_{AgCl} = a + b = 10.\dfrac{2,87}{143,5} = 0,2(2)$
Từ (1)(2) suy ra a = b = 0,1
$m_{NaCl} = 0,1.58,5 = 5,85(gam)$
$m_{KCl} = 0,1.74,5 = 7,45(gam)$
b)
$C\%_{NaCl} = \dfrac{5,85}{500}.100\% = 1,17\%$
$C\%_{KCl} = \dfrac{7,45}{500}.100\% = 1,49\%$

Bạn tham khảo link:
Câu hỏi của Lưu Thùy Trang - Toán lớp 8 | Học trực tuyến
gọi x là nồng độ của dd I
=> C% dd II
m ct của I là 2x
m ct của II là 3x
mà tổng 2 m ct kia sẽ bằng 165 vì trộn 2 dd
=> 2x +3(x-20) = 165
=>x = 45
vậy nồng độ dd I và II lần lượt là 45 và 25

NaBr + AgNO3 \(\rightarrow\)AgBr + NaNO3
NaCl + AgNO3 \(\rightarrow\) AgCl + NaNO3
\(C_M=0,5M\Rightarrow n_{AgNO_3}=0,025\left(mol\right)\)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
\(\Rightarrow x=9,0557.10^{-3};y=0,01594\)
\(\Rightarrow C\%=\frac{0,594.58,5}{50}.100\%=1,865\%\)
NaBr + AgNO3 →→AgBr + NaNO3
NaCl + AgNO3 →→ AgCl + NaNO3
CM=0,5M⇒nAgNO3=0,025(mol)CM=0,5M⇒nAgNO3=0,025(mol)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
⇒x=9,0557.10−3;y=0,01594⇒x=9,0557.10−3;y=0,01594
⇒C%=0,594.58,550.100%=1,865%⇒C%=0,594.58,550.100%=1,865%