Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án D
Gọi hóa trị của kim loại là n (1 ; 2 ; 3), Khối lượng mol là a (g)
Gọi số mol muối mỗi phần là x. Ta có số mol kim loại ban đầu là 2x
Có : 2ax = 4,8 nên ax = 2,4 (1)
Nếu muối tạo thành chỉ là M(NO3)n thì ta có : (a + 62n)x = 25,6 (2)
Từ (1) và (2) => x = (25,6 – 2,4)/(62n) = 0,187/n
Mặt khác , số mol oxit thu được là x/2
=> (2a + 16n).x/2 = 4 (3)
Từ (1) và (3) => x = (4 – 2,4)/(16n) = 0,1/n.
2 giá trị x không bằng nhau. Vì vậy muối phải là muối ngậm nước.
Đặt công thức muối là M(NO3)n.mH2O
Khối lượng muối mỗi phần là (a + 62n + 18m)x = 25,6 (4)
Kết hợp (1), (3), (4) ta có hệ sau :
ax = 2,4
(2a + 16n).x/2 = 4
(a + 62n + 18m)x = 25,6
=> nx = 0,2 ; mx = 0,6
=> a/n = 12. Thay n = 1, 2, 3 ta được a = 24g => Mg
Thay n = 2 => x = 0,1 ; do đó m = 6
Vậy M là Mg và muối là Mg(NO3)2.6H2O

Đáp án : B
* Phân 2 : R2CO3 + CaCl2 à CaCO3↓ + 2RCl
0,04 ß 0,04
* Phần 1 : R2CO3 + Ca(OH)2 à CaCO3↓ + 2ROH
0,04 à 0,04
RHCO3 + Ca(OH)2 à CaCO3↓ +ROH + H2O
0,07 ß (0,11 – 0,04)
=> 0,04(2R + 60) + 0,07(R + 61) = 28,11/3 => R = 18 (NH4+)
* Phần 3 : (NH4)2CO3 + 2NaOH à Na2CO3 + NH3 + 2H2O
0,04 à 0,08
NH4HCO3 + 2NaOH à Na2CO3 + NH3 + 2H2O
0,07 à 0,14
=> nNaOH = 0,14 + 0,08 = 0,22 mol
=> V ddNaOH = 0,22/1 = 0,22 l = 220 ml

Đáp án B
Khối lượng mỗi phần là 28,11/3 = 9,37g
Phần 2 tạo 0,04 mol CaCO3 => nCO32- = 0,04
Phần 1 tạo 0,11 mol CaCO3=> nHCO3- = 0,11 – 0,04 = 0,07
(2R + 60)0,04 + (R + 61)0,07 = 9,37 R = 18 R là NH4
Phần 3:
(NH4)2CO3 +2NaOH -> Na2CO3 + 2NH3 + 2H2O
NH4HCO3 + 2NaOH -> Na2CO3 + NH3 + 2H2O
nNaOH = (0,04 + 0,07).2 = 0,22 V = 0,22 lít

Chọn B
Khối lượng mỗi phần là 28,11/3 = 9,37g
Phần 2 tạo 0,04 mol CaCO3 → nCO32- = 0,04
Phần 1 tạo 0,11 mol CaCO3 → nHCO3- = 0,11 – 0,04 = 0,07
→ (2R + 60)0,04 + (R + 61)0,07 = 9,37
→ R = 18 → R là NH4
Phần 3:
(NH4)2CO3 +2NaOH → Na2CO3 + 2NH3 + 2H2O
NH4HCO3 + 2NaOH → Na2CO3 + NH3 + 2H2O
→ nNaOH = (0,04 + 0,07).2 = 0,22 → V = 0,22 lít

Phản ứng nhiệt nhôm:
![]()
X tác dụng với NaOH thu được => Al dư (*)
Phản ứng xảy ra hoàn toàn (**)
Kết hợp (*), (**) => F e 3 O 4 hết => X gồm Fe, A l 2 O 3 và Al dư
Chú ý: Bài toán chia làm hai phần không bằng nhau
*Xét phần một
Số mol H2 thu được là: ![]()
Trong X, chỉ có Al2O3 và Al dư tác dụng với NaOH theo sơ đồ sau:
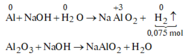
![]()
![]()
Chất rắn thu được là Fe
Chất rắn thu được tác dụng với H2SO4 đặc, nóng:
Sơ đồ phản ứng:
![]()
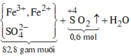
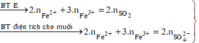
![]()
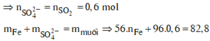
![]()
![]()
![]()
![]()
![]()
![]()
![]()
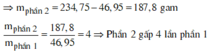
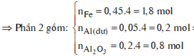
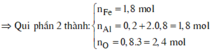
*Xét phần hai:
Số mol HNO3 là: ![]()
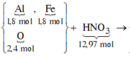
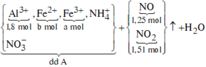
Các quá trình tham gia của H+:
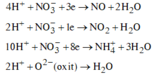
![]()
![]()
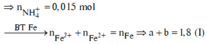
![]()
![]()
![]()


Đáp án A
Tương tự Câu 12, áp dụng định luật bảo toàn mol electron ta có
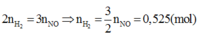
Vậy V= 11,76 (lít)

Đáp án A
Tương tự câu 12, áp dụng định luật bảo toàn mol electron ta có:
2 n H 2 = 3 n N O = > 3 2 n N O = 0 , 525 ( m o l )
Vậy V = 11,76 (lít)

