cho 4,6g 1 kim loại kiềm hòa tan hoàn toàn vào 100g H2O thu đc 4,48l khí ở đktc
a.tìm kim loại
b.tính nồng độ % của dung dịch thu được sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(n_{CuO}=\dfrac{16}{80}=0,2mol\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
b)\(n_{Na}=\dfrac{4,6}{23}=0,2mol\)
\(n_{H_2O}=\dfrac{100}{18}=\dfrac{50}{9}mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(0,2\) \(\dfrac{50}{9}\) 0 0
\(0,2\) 0,2 0,2 0,1
0 \(5,35\) 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)

\(n_K=\dfrac{5,85}{39}=0,15\left(mol\right)\)
PTHH: 2K + 2H2O --> 2KOH + H2
_____0,15------------->0,15-->0,075
=> VH2 = 0,075.22,4 =1,68(l)
mdd = 5,85 + 100 - 0,075.2 = 105,7(g)
=> \(C\%=\dfrac{0,15.56}{105,7}.100\%=7,95\%\)

\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Ta có: \(n_M=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{4,6}{0,2}=23\left(Na\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
0,2......................0,2..........0,1
TH1: HCl dư sau phản ứng
\(NaOH+HCl\rightarrow NaCl+H_2O\)
0,2..............0,2..............0,2
\(m_{NaCl}=0,2.58,5=11,7\) (g) > m chất tan
=> Loại
TH2: NaOH dư
Gọi x là số mol HCl phản ứng
\(NaOH+HCl\rightarrow NaCl+H_2O\)
x.................x.............x
Ta có : \(m_{ct}=\left(0,2-x\right).40+x.58,8=10,96\)
=> x = 0,16
=> \(V=\dfrac{0,16}{1}=0,16\left(l\right)\)

Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)

\(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ 0,3.........0,3.........0,3.......0,3\left(mol\right)\\ m_{ddsau}=16,8+100=116,8\left(g\right)\\ m_{FeSO_4}=152.0,3=45,6\left(g\right)\\ C\%_{ddFeSO_4}=\dfrac{45,6}{116,8}.100\approx39,041\%\)

a)\(n_{HCl}=0,5\cdot1=0,5mol\)
PT: \(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(n_R=\dfrac{4,05}{M_R}\)
\(n_{H_2}=\dfrac{5,04}{22,4}=0,225mol\)
\(\Rightarrow\dfrac{4,05}{M_R}\cdot n=0,225\cdot2\)
R là kim loại:
\(\begin{matrix}n&1&2&3\\M_R&9&18&27\end{matrix}\)
Vậy R có hóa trị III và \(M_R=27\left(Al\right)\)
b)PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,15 0,5 0,225
0,15 0,45 0,15 0,225
Vậy \(C_{M_{AlCl_3}}=\dfrac{0,15}{0,5}=0,3M\)
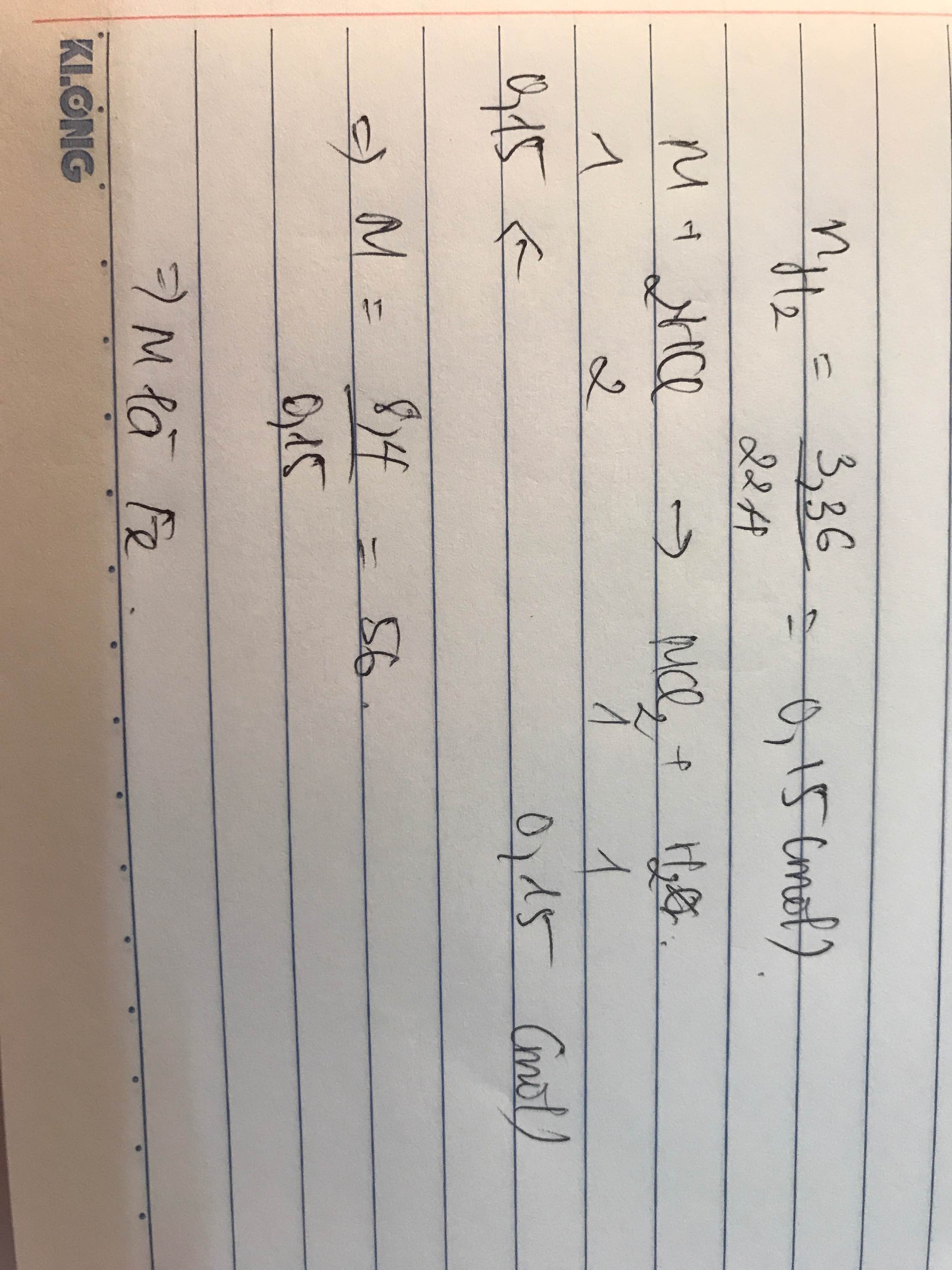
HD: Bài này đề bài phải là 2,24 lít khí ở đktc mới đúng, bạn xem lại đề bài.
Gọi kim loại cần tìm là R.
R + H2O ---> ROH + 1/2H2
a) Số mol R = 2 lần số mol H2 = 2.0,1 = 0,2 mol. Suy ra nguyên tử khối của R = 4,6/0,2 = 23 (Na).
b) Khối lượng dd sau p.ư = 4,6 + 100 - 0,1.2 = 104,4 g. Suy ra C%(NaOH) = 40.0,2/104,4 = 7,66%
ừ chắc mình chép nhầm đề bài ạ