Thủy phân hoà toàn 1 triglixerit X thu đc glixerol và 2 muối của 2 axit béo . Nếu đốt cháy hoàn toàn a mol X thì thu đc 12,768 lít CO2 và 9,54g h2o . Mặt khác a mol X làm mất màu tối đa 40ml dd br2 0,5M. Số nguyên tử H trong chất béo X?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi $n_{O_2} = b(mol)$
Bảo toàn khối lượng :
$m_X = 2,85.44 + 2,6.18 -32b = 172,2 - 32b(gam)$
Mặt khác :
$m_X + m_{NaOH} = m_{muối} + m_{C_3H_5(OH)_3}$
$\Rightarrow 172,2 - 32b + 3a.40 = 45,6 + 92a(1)$
Bảo toàn O :
$6a + 2b = 2,85.2 + 2,6(2)$
Từ (1)(2) suy ra a = 0,05 ; b = 4
Ta có :
$n_{CO_2} - n_{H_2O} = (k-1).n_X \Rightarrow k = 6$
Suy ra số liên kết C = C trong X là 6 - 3 = 3
Suy ra: $n_{Br_2} = x = 3n_X = 0,05.3 = 0,15(mol)$

Chọn đáp án B
Ta có nCO2 = 0,55, nH2O = 0,49 mol
Gọi số liên kết đôi C=C trong gốc axit là k → ak = nBr2 = 0,04 mol
Tổng số liên kết π trong X là π C=C + π C=O = k + 3
Luôn có nCO2 - nH2O = (k + 3-1)a → 0,06 = 0,04+ 2a → a = 0,01 , k= 4
Vì cứ 1 mol X phản ứng với 4 mol Br2 → trong có 2 gốc axit chứa 2 nối đôi ( axit linoleic) và 1 axit no ( Axxit pamitic hoặc axit steatic) → loại A, D
Nhẩm số C = 0,55: 0,01 = 55 = 3 (C3H5) + 16 (C15H31COO)+ 2. 18 (C17H31COO)
Vậy 2 axit béo thu được là axit pamitic và axit linoleic.

Chọn B
Ta có: nX. (kX – 1) = n(CO2) – n(H2O)
→ a. (kX – 1) = 0,55 – 0,49
Lại có: a. (kX – 3) = n(Br2) ((kX – 3) là số pi trong các gốc, do trừ 3COO)
→ a = 0,01 và kX = 7 (=3COO + 4CC)
Ta có: piC-C = 4 có thể phân tích thành: 1 + 2. 2 hoặc 1. 2 + 2
→ Trong các đ.a Tổ hợp 1 axit panmitic và 2 axit linoleic hoặc1 axit steroic và 2 axit linoleic thỏa mãn.
Mặt khác số C trong X = 0,55 : 0,01 = 55 vậy Tổ hợp 1 axit panmitic và 2 axit linoleic thỏa mãn
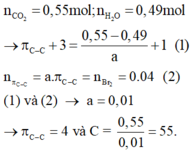

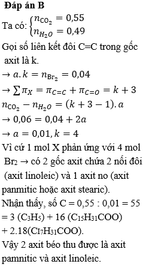

$n_{CO_2} = 0,57(mol) ; n_{H_2O} = 0,53(mol)$
Gọi k số độ bất bão hòa của X
Ta có :
$n_{CO_2} - n_{H_2O} = 0,57 - 0,53 = (k - 1)a$
$n_{Br_2} = a(k-3) = 0,04.0,5 = 0,02$
Suy ra: ak = 0,05; a = 0,01
Số nguyên tử H trong X là $2n_{H_2O} : n_X =106$
Xem lại đề đi e, số mol $H_2O$ tính ra lẻ quá