Nguyên tử của nguyên tố X có 4 lớp electron, số electron ở lớp ngoài cùng là 7. Tỉ số giữa số hạt không mang điện và số hạt mang điện là 0,6429.
a. Tìm số điện tích hạt nhân và số khối của X
b. Nguyên tử của nguyên tố R có số nơtron bằng 53,143% số proton của X.
c. Vẽ sơ đồ cấu tạo của nguyên tử, số lớp e, số e lớp ngoài cùng?

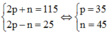





XX có 4 lớp electron.
Ta có lớp 1 có tối đa 2 ee.
Lớp 2 có tối đa 8 ee.
Lớp 3 có tối đa 18 ee.
Lớp 4 của nguyên tố này có 7 ee
Do vậy XX chứa số ee là
eX=2+8+18+7=35eX=2+8+18+7=35
Trong một nguyên tử ta luôn có:
pX=eX=35pX=eX=35
Trong nguyên tử, hạt mang điện là p;ep;e; không mang điện là nn
→np+e=n35.2=0,6429→n=45→np+e=n35.2=0,6429→n=45
Hạt nhân của XX chứa 35 pp nên điện tích hạt nhân là 35+.
Số khối của XX
Nguyên tố RR có số nn là
AX=p+n=35+45=80 (u)AX=p+n=35+45=80 (u)
nR=53,143%pX=18,6nR=53,143%pX=18,6 (phần này xem lại đề)
Câu cc hỏi cấu tạo nguyên tử gì em??
Nếu là XX thì cấu tạo như này
Câu tạo của XX có 4 lớp e và 7e ngoài cùng.