

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án C
Gọi số khối của ba đồng vị tương ứng x1, x2, x3
Ta có x2= x1 +1
Theo đề ra ta có hệ phương trình
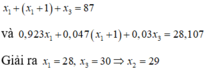

Tổng số khối 3 đồng vị X1,X2,X3 là 87 nên ta có pt:
\(A_{X1}+A_{X2}+A_{X3}=87\left(1\right)\)
Vì X2 có nhiều hơn X1 là 1 hạt notron, nên ta có pt:
\(N_{X2}-N_{X1}=1\\ \Leftrightarrow A_{X2}-A_{X1}=1\left(2\right)\)
Mặt khác, khối lượng nguyên tử trung bình là 28,0855 đ.v.C nên ta có pt:
\(\dfrac{A_{X1}.92,23\%+A_{X2}.4,67\%+A_{X3}.3,1\%}{100\%}=28,0855\left(đ.v.C\right)\left(3\right)\)
Từ (1), (2), (3) ta lập được hệ 3pt và giải tìm nghiệm được:
\(\left\{{}\begin{matrix}A_{X1}\approx28\left(đ.v.C\right)\\A_{X2}\approx29\left(đ.v.C\right)\\A_{X3}\approx30\left(đ.v.C\right)\end{matrix}\right.\)
\(b.\left\{{}\begin{matrix}P_{X1}+N_{X1}=28\\P_{X1}=N_{X1}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P_{X1}=14\\N_{X1}=14\end{matrix}\right.\\ \Rightarrow N_{X2}=29-14=15\left(hạt\right)\\ N_{X3}=30-14=16\left(hạt\right)\)

A = 92,23%X1 + 4,67%X2 + 3,1%X3 = 28,0855
Tổng số khối = X1 + X2 + X3 = 87
X1 + 1 = X2
—> X1 = 28; X2 = 29; X3 = 30

1.Ta có: 2p+n1=54 ; 2p+n2=52
=>P=17=>n1=20=>n2=18
=>R=0,25∗37+0,75∗35=35,5
2
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 82:
p + e + n = 82 hay 2p + n = 82 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 22 hạt
(p+e) – n = 22 hay 2p – n = 22 (2)
Giải (1), (2) ta có p = e = 26; n =30
Số khối của X = Z + N = p + n =56
Bài 2:
a: Theo đề, ta có:
\(\left\{{}\begin{matrix}2Z+N=82\\Z-N=-4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3Z=78\\Z-N=-4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=26\\N=Z+4=30\end{matrix}\right.\)
A=26+30=56
b: Y: \(^{56}_{26}Fe\)

_Tổng số khối của ba đồng vị là 87:
=>X(1) + X(2) + X(3) = 87(1)
_Số notron trong đồng vị II hơn đồng vị I là 1 hạt:
=>N(2) - N(1) = 1
=>X(2) - X(1) = 1(2)
_Nguyên tử khối trung bình của X là ≈ 28.1:
=>M(tb) = (92.23X(1) + 4.67X(2) + 3.1X(3)) / 100 = 28.1
<=>92.23X(1) + 4.67X(2) + 3.1X(3) = 2810(3)
Từ(1)(2)(3) => X(1) = 28, X(2) = 29, X(3) = 30

Vì phần trăm các đồng vị bằng nhau nên mỗi đồng vị chiếm 50%.
Vì các loại hạt trong X1 bằng nhau và X1 có tổng số hạt (gồm p, n, e) là 18
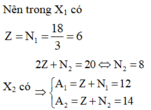
Vậy nguyên tử khối trung bình của X là:
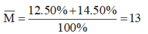
Đáp án D

Đáp án D.
X1 có tổng các loại hạt bằng = 18 và các hạt trong X1 bằng nhau
Ta có p + e + n = 18 mặt khác p = e =n
=> p = e = n =6
X2 có số hạt proton bằng số hạt proton trong X1 do cùng là đồng vị:
2p + n =20 => n = 8
Ta có số khối của X1 = 12, X2 = 14 và %X1 = %X2 = 50%.
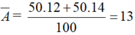

Đáp án D
Vì phần trăm các đồng vị bằng nhau nên mỗi đồng vị chiếm 50%.
Vì các loại hạt trong X1 bằng nhau và X1 có tổng số hạt (gồm p, n, e) là 18
Nên trong X1 có Z = N 1 = 18 3 = 6
X2 có 2 Z + N 2 = 20 ⇔ N 2 = 8 ⇒ A 1 = Z + N 1 = 12 A 2 = Z + N 2 = 14
Vậy nguyên tử khối trung bình của X là:
M
¯
=
12
.
50
%
+
14
.
50
%
100
%
=
13