Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2yAl + 3FexOy ---> yAl2O3 + 3xFe (1) Chất rắn B gồm Al2O3, Fe và Al dư (vì phản ứng xảy ra hoàn toàn nên FexOy không dư).
0,08 0,04 0,08
Al(dư) + NaOH + H2O ---> NaAlO2 + 3/2H2 (2)
0,02 0,02 0,03 mol
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O (3) Phần không tan D là Fe.
NaAlO2 + HCl + H2O ---> Al(OH)3\(\downarrow\)+ NaCl (4)
2Al(OH)3 ---> Al2O3 + 3H2O (5) (5,1 gam chất rắn là Al2O3).
0,1 0,05 mol
2Fe + 6H2SO4 ---> Fe2(SO4)3 + 3SO2\(\uparrow\) + 6H2O (6)
0,08 0,12 mol
Theo pt(4) và (5) số mol NaAlO2 = số mol Al(OH)3 = 0,1 mol. Do đó số mol NaAlO2 ở pt (3) = 0,1 - 0,02 = 0,08 mol. Suy ra số mol Al2O3 sinh ra ở pư (1) = 0,04 mol.
Theo pt(6) số mol Fe = 0,08 mol. Như vậy, từ pt (1) ta có: 2y = 3x hay x/y = 2/3. Suy ra: Fe2O3.
m = mAl + mFe2O3 = 27(0,08 + 0,02) + 160.0,04 = 9,1 gam.

Đáp án B
P1 : + NaOH có khí H2 => Al dư , FexOy hết
=> mFe = 5,04g => nFe = 0,09 mol ; nAl dư = 0,03 mol = 2/3nH2
=> nFe + nAl = 0,12 mol
P2 : Fe và Al phản ứng tạo NO => nFe + nAl = nNO (bảo toàn e) = 0,36 mol = 3nP1
=> mP1 = 1/3mP2 = 9,93g => m = 9,93 + 29,79 = 39,72g
Xét P1 : mAl2O3 + mFe + mAl = mP1 = 9,93g => nAl2O3 = 0,04 mol => nO = 0,12 mol
=> nFe : nO = 0,09 : 0,12 = 3 : 4 => Fe3O4
=>B

Gọi nAl=x mol và nFe2O3 = y mol
Fe2O3 + 2Al → Al2O3 + 2Fe
Đầu(mol) y x
Do chất rắn sau +NaOH tạo khí nên dư Al
=> nH2=1,5nAl => 0,06= x-a mX= 160y + 27x = 21,67
m rắn không tan = mFe2O3 + mFe = 160(y – ½ a) + 56a=12,4
Giải hệ : x=0,21mol ; y=0,1mol ; a =0,15mol.
Tính hiệu suất theo Fe2O3 => %H= (0,075/0,1) .100%= 75%
=>D


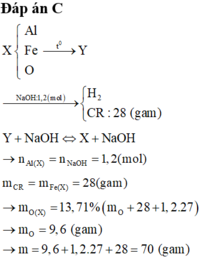



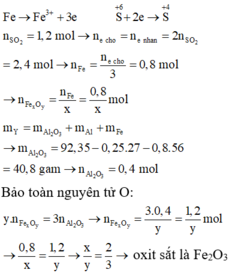
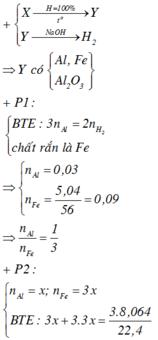
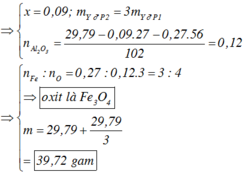
Chọn B.