Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
viết phương trình điện ly của các chất sau : K2S , Na2HPO4 , NaH2PO4 , Pb(OH)2 , HBrO , HF , HClO4 .

Phân trình điện li:
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-H2PO4- H+ + HPO42-HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.

Phương trình điện li :
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-
HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơ
H2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
a/ K2S -> 2K+ S2_
b/ Na2HPO4 -> 2Na +. HPO42-HPO42- H + + PO43-
c/ NaH2PO4 -> Na + + H2PO4-H2PO4 - H+ + HPO42-HPO42- H+ + PO43-
d/ Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e/ HBrO H+ + BrO-
g/ HF H+ +F-
h/ HCIO4 -> H+ +CIO4-

a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-H2PO4- H+ + HPO42-HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơH2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.
K2S 2K+ + S2-
Na2HPO4 2Na+ + HPO42-
HClO4 H+ +ClO4-
Pb(OH)2 Pb2+ + 2OH-
Pb(OH)2 2H+ + PbO22-
HF H+ +F-
HPO42- H+ + PO43-
NaH2PO4 Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
HBrO H+ + BrO-

Phương trình điện li :
a) K2S → 2K+ + S2_
b) Na2HPO4 → 2Na+ +. HPO42-
HPO42- H+ + PO43-
c) NaH2PO4 → Na+ + H2PO4-
H2PO4- H+ + HPO42-
HPO42- H+ + PO43-
d) Pb(OH)2 Pb2+ + 2OH- : phân li kiểu bazơ
H2PbO2 2H+ + PbO22- : phân li kiểu axit
e) HBrO H+ + BrO-
g) HF H+ + F-
h) HClO4 → H+ + ClO4-.

H3PO4 + K2HPO4 →2KH2PO4
H3PO4 + Ca(OH)2 →CaHPO4 +2H2O
2H3PO4 + 3Ca(OH)2 →Ca3(PO4)2 +6H2O

Lấy ở mỗi lọ 1 ml các dd lm mẫu thử
-Cho QT vào các MT
+MT lm QT hóa xanh là Ba(OH)2
+MT Lm QT hóa đỏ là H3PO4
+MT K làm QT chuyển màu là (NH4)2SO4 và Na2SO4
Cho Ba(OH)2 vào (NH4)2SO4 và Na2SO4
MT xuất hiện kết tủa trắng là Na2SO4
Na2SO4+Ba(OH)2---->2NaOH+BaSO4
Mt xuất hiện kết tủa và khí là (NH4)2SO4
(NH4)2SO4+Ba(OH)2---->BaSO4+2NH3+H2O
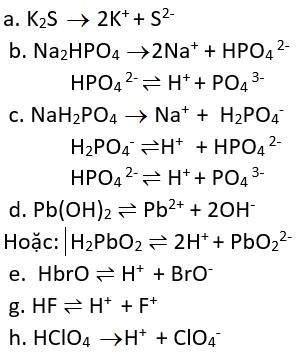

Viết phương trình điện li của các chất sau đây trong dung dịch :
1. Axit mạnh H2SeO4 (nấc thứ nhất điện li mạnh)
\(H_2SeO_4\rightarrow H^++HSeO_4^-\)
\(HSeO_4^-\leftrightarrow H^++SeO_4^{2-}\)
2. Axit yếu 3 nấc H3PO4
\(H_3PO_4\leftrightarrow H^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
3. Hiđroxit lưỡng tính Pb(OH)2
\(Pb\left(OH\right)_2\leftrightarrow Pb^{2+}+2OH^-\)
\(Pb\left(OH\right)_2\leftrightarrow PbO_2^{2-}+2H^+\)
4. Na2HPO4
\(Na_2HPO_4\leftrightarrow2Na^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
5. NaH2PO4
\(NaH_2PO_4\leftrightarrow Na^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
6. Axit mạnh HMnO4
\(HMnO_4\rightarrow H^++MnO_4^-\)
7. Bazơ mạnh RbOH
\(RbOH\rightarrow Rb^++OH^-\)