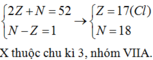Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cation R+ có cấu hình electron 1s22s22p63s23p6 Cấu hình electron của R là 1s22s22p63s23p64s1 (Z=19) →R là nguyên tố Kali thuộc chu kì 4, nhóm IA.
Chọn đáp án D

Chọn đáp án B.
- Anion X- có cấu hình electron lớp ngoài cùng là 3s23p6 → Cấu hình electron lớp ngoài cùng của X là 3s23p5 X là Cl (Z = 17) thuộc chu kì 3, nhóm VIIA.
- Cation Y2+có cấu hình electron lớp ngoài cùng là 3s23p6 → Cấu hình electron lớp ngoài cùng của Y là 3p64s2 → Y là Ca (Z = 20) thuộc chu kỳ 4, nhóm IIA.

Chọn đáp án B.
Dễ dàng nhìn thấy L- , E2- , T, M+ đều có cùng cấu hình electron của khí hiếm Ar.

Nhận thấy: 8 = 6 + 2 → Cấu hình electron của X là 1s22s22p63s23p2 (Z=14)→Xlà nguyên tố Silic (Si).
Chọn đáp án D

Chọn đáp án C.
Dựa vào cấu hình electron của X và Y ta suy ra X là K (Z = 19) và Y là F (Z = 9) → Liên kết giữa Kali và Flo là liên kết giữa kim loại điển hình và phi kim điển hình → Liên kết ion.