
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

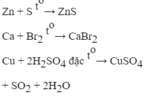

Gọi nK2O=a, nMgO=b trong 8g hh
K2O + H2SO4 \(\rightarrow\) K2SO4 + H2O
a \(\rightarrow\) a (mol)
MgO + H2SO4 \(\rightarrow\) MgSO4 + H2O
b \(\rightarrow\) b (mol)
K2SO4 + 2NaOH \(\rightarrow\) Na2SO4 + 2KOH
MgSO4 + 2NaOH \(\rightarrow\) Na2SO4 + Mg(OH)2
b \(\rightarrow\) b (mol)
nMg(OH)2 = \(\frac{2,9}{58}\) = 0,05 (mol)
\(\Rightarrow\) b = 0,05 (mol)
\(\Rightarrow\) %mMgO = \(\frac{0,05.40}{8}\) . 100% = 25%
%mK2O = 75%

+ Cho A tác dụng với dd NaOH dư:
Chất rắn A1: Fe3O4, Fe; dd B1: NaAlO2 và NaOH dư; khí C1: H2
+ Cho khí C1 tác dụng với A1
Fe3O4 + 2H2 ---> 3Fe + 4H2O.
Chất rắn A2: Fe, Al, Al2O3
+ Cho A2 tác dụng H2SO4 đặc nguội.
Al2O3+ 3H2SO4---->Al2(SO4)3+3H2O
Dd B2: Al2(SO4)3
+ Cho B2 tác dụng với dd BaCl2
Al2(SO4)3+ 3BaCl2--->2AlCl3+3BaSO4
B3: BaSO4
Xác định được các chất: A1, A2, B1, B2, B3, C1

a) H2SO4 + NạOH → H2O + NaHSO4
b) H2SO4 + 2NaOH → 2H2O + Na2SO4

a, Mg + 2HCl \(\rightarrow\) MgCl2 + H2 Cu + 2HCl \(\rightarrow\) CuCl2 + H2
b, \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Cu}=y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}24x+64y=16\\x+y=\dfrac{2,24}{22,4}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=-0,24\\y=0,34\end{matrix}\right.\)
Xem lại đầu bài nha

Fe + S → t ∘ FeS
S + O2 → t ∘ SO2
FeS + O2 → t ∘ Fe2O3 + SO2

a) (-) Nhôm và oxi Lấy bột nhôm bỏ vào 1 miếng bìa cứng . Khum tờ giấy chứa bột nhôm , rắc nhẹ bột nhôm trên ngọn lửa đèn cồn .
Hiện tượng: Có những hạt loé sáng do bột nhôm tác dụng với oxi, phản ứng toả nhiều nhiệt.
Chất tạo thành màu trắng sáng là nhôm oxit Al2O3
Giải thích: Vì xảy ra phản ứng nhôm tác dụng với oxi trong không khí.
(-) Sắt và lưa huỳnh Trộn bột sắt và bột lưa huỳnh rồi cho vào ống nghiệm ,Hơ ống nghiệm trên đèn cồn .
Hiện tượng: Khi đun hỗn hợp trên ngọn lửa đèn cồn, sắt tác dụng mạnh với lưu huỳnh hỗn hợp cháy nóng đỏ, phản ứng toả nhiều nhiệt.
Chất tạo thành có màu đen (không bị nam châm hút).
Giải thích: Vì xảy ra phản ứng sắt tác dụng với lưu huỳnh.
b) PTHH : 4Al + 3O2 → Al2O3→ Trong PƯHH nhôm đóng vai trò là chất khử.
PTHH : Fe + S → → FeS Hỗn hợp sắt và lưu huỳnh trước phản ứng có màu xám.
a)
(+) Nhôm và oxi
Lấy bột nhôm bỏ vào 1 miếng bìa cứng . Khum tờ giấy chứa bột nhôm , rắc nhẹ bột nhôm trên ngọn lửa đèn cồn .
(+) Sắt và lưa huỳnh
Trộn bột sắt và bột lưa huỳnh rồi cho vào ống nghiệm ,Hơ ống nghiệm trên đèn cồn .
b)
PTHH :
4Al + 3O2 \(\rightarrow\) 2Al2O3
PTHH :
Fe + S \(\rightarrow\) FeS
P/s : Em ms lp 8 nên ko bt đúng hay sai