Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có :
\(\%H_2O = \dfrac{18n}{M + 62.3 + 18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ %N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2)\Rightarrow M = 56(Sắt) ; n = 9\)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)
\(\%H_2O= \dfrac{18n}{M + 62.3+18n}.100\% = 40,099\%\\ \Rightarrow M + 62.3 = \dfrac{242}{9}n(1)\\ \%N = \dfrac{14.3}{M + 62.3 + 18n}.100\% = 10,4\%\\ \Rightarrow M + 18n = \dfrac{2832}{13}(2)\\ (1)(2) \Rightarrow M = 56(Sắt) ; n = 9\\ \)
CTHH cần tìm : \(Fe(NO_3)_3.9H_2O\)

Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
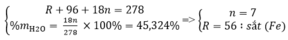
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O

1/ CTHH dạng TQ là ASO4 . xH2O
*Có : %S/muối tinh thể = \(\dfrac{1.M_S}{M_{ASO4.xH2O}}.100\%=11,51\%\)
=> \(\dfrac{32}{M_{ASO4.xH2O}}=0,1151\)
=> MASO4.xH2O = 278(g)
* Có : %H2O/muối tinh thể = \(\dfrac{x.M_{H2O}}{M_{ASO4.xH2O}}.100\%=45,32\%\)
=> \(\dfrac{x.18}{278}=0,4532\)
=>x= 7
*Lại có : MASO4.xH2O = 278
mà x = 7
=> MA + 96 + 7 .18=278 => MA =56(g) => A là Sắt (Fe)
Vậy CTPT của tinh thể là FeSO4 .7H2O

Giải:
Đặt công thức của muối sunfat ngậm nước là:
ASO4. nH2O (n ∈ N*)
Theo bài ra ta có:
Cứ 32g S chiếm 11,51%
Vậy MASO4.nH2O chiếm 100%
=> mASO4. nH2O =\(\dfrac{32.100\%}{11,51}\) = 278 (g) (1)
*Mặt khác ta có:
\(\dfrac{18n}{278}\) = \(\dfrac{45,52}{100}\)
⇔ 18n . 100 = 278 . 45,52
⇔ 18n . 100 = 12654,56
⇔ 18n = 12654,56 : 100
⇔ 18n = 126,5456
⇔ n = 126,5456 : 18
⇔ n = 7 (TMĐK) (2)
Từ (1) và (2) ta có:
MASO4 . 7H2O = NTK(A) + 32 + 16.4 + 7.18 = 278
⇔ NTK(A) + 222 = 278
⇔ NTK(A) = 278 - 222
⇔ NTK(A) = 56 (đvC)
Vậy A là Sắt (Fe)
CT của tinh thể là FeSO4 . 7H2O
Đặt tên công thức ko nhất định phải là MSO4. nH2O mà các bn có thể đặt tên kim loại tùy ý nha

CTHH: R(NO3)2.xH2O (A)
\(\%m_{NO_3^-}=100\%-42,1875\%-9,375\%=48,4375\%\)
Xét \(\dfrac{m_R}{m_{NO_3^-}}=\dfrac{1.M_R}{2.62}=\dfrac{9,375\%}{48,4375\%}\)
=> MR = 24 (g/mol)
=> R là Mg
(A) có CTHH là Mg(NO3)2.xH2O
Có: \(\%m_{H_2O}=\dfrac{18x}{148+18x}.100\%=42,1875\%\)
=> x = 6
=> CTHH: Mg(NO3)2.6H2O

CTHH: R(OH)2.xH2O
\(\%m_{OH}=100\%-24\%-60,88\%=15,12\%\)
Xét \(\dfrac{m_R}{m_{OH}}=\dfrac{60,88\%}{15,12\%}=\dfrac{761}{189}\)
=> \(\dfrac{1.M_R}{2.17}=\dfrac{761}{189}\)
=> MR = 137 (g/mol)
=> R là Ba
=> CTHH: Ba(OH)2.xH2O
Có: \(\%H_2O=\dfrac{18x}{171+18x}.100\%=24\%\)
=> x = 3
=> CTHH: Ba(OH)2.3H2O

bài này nếu 9h tốiko ai làm thì mk sẽ làm cho nha
chuẩn bị ăn cơm
thôi,làm liều!!!
Gọi CTHH của tinht thể là \(R\left(NO_3\right)_3.nH_2O_{ }\)
ta có %mH2O=40,099%
=> \(\dfrac{18n}{18n+M_R+186}=0,40099\)
Mặt khác %mN= 10,396%
=> \(\dfrac{14.3}{18n+M_R+186}=\dfrac{2599}{25000}\)
=> \(18n+M_R+186\approx404\)
=> \(18n=404.0,40099\approx162=>n=9\)
\(18.9+M_R+186=404=>M_R=56\left(Fe\right)\)
vậy CTHH là \(Fe\left(NO_3\right)_3.9H_2O\)

Gọi công thức tinh thể là: \(M_2CO_3.nH_2O\)
Thành phần nước kết tinh chiếm 47,73 % nên ta có
\(\dfrac{18n}{2M+60+18n}=0,4773\)
\(\Leftrightarrow4773M-47043n+143190=0\left(1\right)\)
Khối lượng nguyên tố Oxi trong tinh thể là: \(16.3+16n=48+16n\)
\(\Rightarrow\dfrac{48+16n}{2M+60+18n}=0,1818\)
\(\Leftrightarrow909M-31819n-92730=0\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}4773M-47043n+143190=0\\909M-31819n-92730=0\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}n\approx-5\\M\approx-82\end{matrix}\right.\)
Chả biết cái đề sai hay mình sai nữa
Gọi công thức tinh thể muối ngaanm nước cần tìm là (M_2CO_3.nH_2O)
Theo đề, thành phần nước kết tinh chiếm 47,73%
Ta có: (dfrac{18n.100}{2M+60+18n} = 47,73)
(<=> 95,46M + 2863,8 + 859,14n = 1800)
(<=> 95,46M - 940,86n = -2863,8 ) ((I))
Trong tinh thể chứa 18,18 % nguyên tố oxi
Ta có: (dfrac{3.16.100}{2M+60+18n}=18,18)
(<=> 36,36M + 1090,8 + 327,24n = 4800 )
(<=> 36,36M + 327,24n = 3709,2) ((II))
Từ ((I))và ((II))Ta có (left{egin{matrix}95,46M-940,86n=-2863,8\36,36M+327,24n=3709,2end{matrix} ight.)
(<=> ) (left{egin{matrix}M=39\n=7end{matrix} ight.)
Vậy M là Kali. KHHH: K
=> Công thức : (K_2CO_3.7H_2O)
1/ CTHH dạng TQ là ASO4 . xH2O
%S tinh thể =\(\frac{1.M_S}{M_{ASO4.xH2O}}.100\%=11,5\%\)
=> \(\frac{32}{M_{ASO4.xH2O}}=0,115\)
=> MASO4.xH2O = 278(g)
% H2O kết tinh = \(\frac{x.M_{H2O}}{M_{ASO4.xH2O}}.100\%=45,34\%\)
=> \(\frac{x.18}{287}=0,4534\)
=>x= 7
MASO4.xH2O = 278
mà x = 7
=> MA + 96 + 7 .18=278
=> MA =56(g) => A là Sắt (Fe)
Vậy CTPT của tinh thể là FeSO4 .7H2O
Chúc bạn học tốt