Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: 2,4 gam hỗn hợp X: \(\left\{{}\begin{matrix}CuO:a\left(mol\right)\\RO:b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow80a+2Ra+32a=2,4\left(I\right)\)
*TH1: Oxit của kim loại R bị khử bởi CO tạo thành kim loại R
\(CuO\left(a\right)+CO-t^o->Cu\left(a\right)+CO_2\)
\(RO\left(2a\right)+CO-t^o->R\left(2a\right)+CO_2\)
\(3Cu\left(a\right)+8HNO_3\left(\dfrac{8a}{3}\right)\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(3R\left(2a\right)+8HNO_3\left(\dfrac{16a}{3}\right)\rightarrow3R\left(NO_3\right)_2+2NO+4H_2O\)
\(\Rightarrow\dfrac{8a}{3}+\dfrac{16a}{3}=0,1\)
\(\Rightarrow a=0,0125\left(mol\right)\)
Thay vào (I) => R = 40 (loại)
* TH2: Kim loại R không bị khử bởi CO
\(CuO\left(a\right)+CO-t^o->Cu\left(a\right)+CO_2\)
\(3Cu\left(a\right)+8HNO_3\left(\dfrac{8a}{3}\right)\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(RO\left(2a\right)+2HNO_3\left(4a\right)\rightarrow R\left(NO_3\right)_2+H_2O\)
\(\Rightarrow\dfrac{8a}{3}+4a=0,1\)
\(\Rightarrow a=0,015\left(mol\right)\)
Thay vào (I) => R = 24 (Mg)
Vậy kim loại R chưa biết là Mg

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
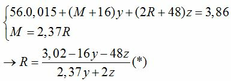
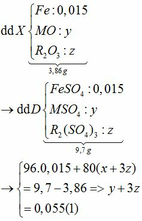
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


Cho hỗn hợp X vào H2SO4 thu được (a+b)g --> hh X gồm oxit kim loại A và kim loại B
Trong đó: oxit kim loại A ko bị khử bởi CO, kim loại B ko tan trong d.d H2SO4
-->Dễ suy ra kim loại B là Cu
(*)Giả sử oxit kim loại A là AO
AO+H2SO4-->ASO4+H2O
1..........1..........1 mol
m d.d sau pư=A+16+980=A+996 g
C% ASO4=11,765%
\(\Rightarrow\frac{A+96}{A+996}=0,11765\)
\(\Rightarrow A=24\left(Mg\right)\)
(*) Giả sử là A2O3 làm tương tự -->loại
Nếu ko chia trường hợp thì gọi là A2Ox hoặc AxOy


Gọi kim loại là M
Ta có nCuO = a, nMO = 2a
CuO + CO-t0-> Cu + CO2
MO + CO --t0---> M + CO2
3Cu + 8HNO3---> 3Cu(NO3)2 + 2NO + 4H2O
3M + 8HNO3 ---> 3M(NO3)2 + 2NO +4H2O
Ta có mhh= 80a + 2a( M + 16)=2,4
<=> 80a + 2aM+ 32a= 2,4
<=>112a + 2aM= 2,4(1)
Lại có nHNO3 = 2,5.0,04=0,1 = 8/3 nCu + 8/3. nM
= 8a/3 + 8/3.2a=8a
<=> a=0,0125 ( 2)
thay (2) vào (1) ta có M=40g /mol
vậy M là Ca
bai nay xay ra hai truong hop nha