Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)

H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé

Đáp án A
Số mol các chất là:
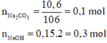
Na2CO3 tác dụng với dung dịch HCl dư:
Sơ đồ phản ứng:
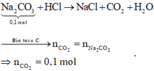
Xét giai đoạn hấp thụ CO2 vào dung dịch NaOH:
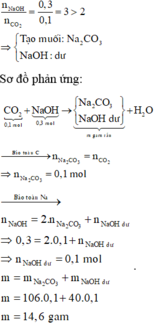

1)
- TN1:
\(n_{AgCl}=\dfrac{35,875}{143,5}=0,25\left(mol\right)\)
PTHH: AgNO3 + HCl --> AgCl + HNO3
0,25<--0,25
TN2:
nNaOH = 0,5.0,3 = 0,15 (mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,15--->0,15
\(n_{HCl\left(dd.C\right)}=0,25+0,15\) = 0,4 (mol)
=> \(C_{M\left(dd.C\right)}=\dfrac{0,4}{2}=0,2M\)
2)
Có \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{V}M\\C_{M\left(B\right)}=\dfrac{0,15}{V^,}M\end{matrix}\right.\)
nHCl(A) = \(\dfrac{0,025}{V}\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
\(\dfrac{0,025}{V}\)------>\(\dfrac{0,0125}{V}\)
nHCl(B) = \(\dfrac{0,015}{V^,}\) (mol)
PTHH: Fe + 2HCl --> FeCl2 + H2
\(\dfrac{0,015}{V^,}\)-------->\(\dfrac{0,0075}{V^,}\)
TH1: \(\dfrac{0,0125}{V}=\dfrac{0,0075}{V^,}+0,02\)
Mà V + V' = 2 (l)
=> \(\left[{}\begin{matrix}V=1,5;V^,=0,5\left(KTM\right)\\V=0,5;V^,=1,5\left(TM\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{0,5}=0,5M\\C_{M\left(B\right)}=\dfrac{0,15}{1,5}=0,1M\end{matrix}\right.\)
TH2: \(\dfrac{0,0125}{V}+0,02=\dfrac{0,0075}{V^,}\)
=> \(\left[{}\begin{matrix}V=\dfrac{1+\sqrt{6}}{2};V^,=\dfrac{3-\sqrt{6}}{2}\\V=\dfrac{1-\sqrt{6}}{2}\left(L\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{\dfrac{1+\sqrt{6}}{2}}=\dfrac{-1+\sqrt{6}}{10}M\\C_{M\left(B\right)}=\dfrac{0,15}{\dfrac{3-\sqrt{6}}{2}}=\dfrac{3+\sqrt{6}}{10}M\end{matrix}\right.\)

nSO2 = 4.48/22.4 = 0.2 (mol)
nNaOH = 0.15*2 = 0.3 (mol)
nNaOH / nSO2 = 0.3 / 0.2 = 1.5
=> Tạo ra 2 muối
Đặt :
nNa2SO3 = x mol
nNaHSO3 = y mol
=> 2x + y = 0.3
x + y = 0.2
=> x = y = 0.1
mNa2SO3 = 0.1*126 = 12.6 (g)
mNaHSO3 = 0.1*104 = 10.4 (g)
nNaOH= 0,3(mol); nSO2=0,2(mol)
Ta có: 2>nOH-/nSO2=0,3/0,2=1,5>1
=> Sản phẩm là hỗn hợp 2 muối: Na2SO3 và NaHSO3
PTHH: 2 NaOH + SO2 -> Na2SO3 + H2O
2x____________x_____x(mol)
NaOH + SO2 -> NaHSO3
y_______y______y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=> m(muối)=mNa2SO3+ mNaHSO3= 126x+104y=126.0,1+104.0,1=23(g)
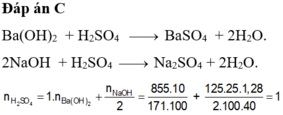
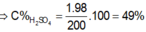
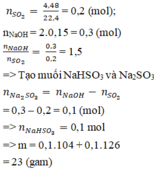
m dd sau trộn = 150 + 460 = 610 g.
mNaOH sau trộn = 150. 10% + 460.x% = 15 + 4,6x (g)
Ta có 15 + 4,6 x = 610. 6% => x \(\approx\)4,7%
tinh the nào ra 4,7 vậy