
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

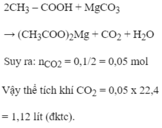

Bài 1:
nHCl = 0,5 . 0,2 = 0,01 mol
nH2SO4 = 0,25 . 0,2 = 0,05 mol
Pt: Na2O + H2O --> 2NaOH
.....0,055<-----------(0,01 + 0,1)....(mol)
.....NaOH + HCl --> NaCl + H2O
....0,01<----0,01..............................(mol)
.....2NaOH + H2SO4 --> Na2SO4 + 2H2O
......0,1<------0,05............................................(mol)
mNaOH = 0,055 . 40 = 2,2 (g)
Bài 2:
nH2SO4 = 1,1 . 0,1 = 0,11 mol
nNaOH = 1 . 0,1 = 0,1 mol
nAl = \(\dfrac{1,35}{27}=0,05\left(mol\right)\)
Pt: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
.....0,05 mol-> 0,1 mol
Xét tỉ lệ mol giữa NaOH và H2SO4:
\(\dfrac{0,1}{2}< \dfrac{0,11}{1}\)
Vậy H2SO4 dư
nH2SO4 dư = 0,11 - 0,1 = 0,01 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
................0,01 mol-------------------> 0,01 mol
Xét tỉ lệ mol giữa Al và H2SO4:
\(\dfrac{0,05}{2}>\dfrac{0,01}{3}\)
Vậy Al dư
VH2 thu được = 0,01 . 22,4 = 2,24 (lít)

bạn vô trang hóa này đi sẽ có nhiều người giúp bạn https://www.facebook.com/groups/1515719195121273/

a) CaCO3+2HCl=>CaCl2+H2O+CO2
n CaCO3=10/100 = 0,1 mol
theo phương trình : n CO2 = n CaCO3 = 0,1 mol
=> V CO2 = 0,1*22,4 = 2,24 lít
b) CO2+2NaOH => Na2CO3+H2O
có thể xảy ra phản ứng :
Na2CO3+CO2+H2O=>2NaHCO3
m NaOH = 25*0,4 = 10 gam
=> n NaOH = 10/40 = 0,25 mol
mà nếu theo phương trình đầu tiên của câu b:
n CO2 = 1/2 n NaOH = 1/2*0,25 = 0,125 mol
mà thực tế n CO2 có 0,1 mol
=> n CO2 hết, n NaOH dư
=> chỉ tạo ra 1 muối là Na2CO3
n Na2CO3 = n CO2 = 0,1 mol
=> m Na2CO3 = 0,1*106=10,6 gam

3)\(n_{H_2}\)=4,48:22,4=0,2(mol)
=>\(m_{H_2}\)=0,2.2=0,4(mol)
Gọi n là hóa trị của R
Ta có PTHH:
2R+nH2SO4->R2(SO4)n+nH2
........................2R+96n......2n..........(g)
.........................22,8..........0,4..........(g)
Theo PTHH:0,4(2R+96n)=2n.22,8
=>0,8R+38,4n=45,6n=>0,8R=7,2n
=>R=9n
Vì R là hóa trị của R nên n\(\in\){1;2;3}
Biện luận:
| n | 1 | 2 | 3 |
| R | 9 | 18 | 27 |
=>n=3;R=27(Al) là phù hợp
Vậy R là Al
3) \(CuO+H_2\rightarrow Cu+H_2O\left(1\right)\)
\(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\left(2\right)\)
Cu không phản ứng với HCl
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(3\right)\)
\(n_{H_2}=\dfrac{\dfrac{448}{1000}}{22,4}=0,02\left(mol\right)\)
Theo(3):\(n_{Fe}=n_{H_2}=0,02\left(mol\right)\)
\(m_{Fe}=0,02.56=1,12\left(g\right)\)
\(m_{Cu}=1,76-1,12=0,64\left(g\right)\)
\(n_{Cu}=\dfrac{0,64}{64}=0,01\left(mol\right)\)
\(n_{CuO}=n_{Cu}=0,01\left(mol\right)\)
\(m_{CuO}=0,01.80=0,8\left(g\right)\)
\(m_{Fe_xO_y}=2,4-0,8=1,6\left(g\right)\)
Theo (2):\(n_{Fe_xO_y}=\dfrac{0,02}{x}\)
Theo đề bài:\(n_{Fe_xO_y}=\dfrac{1,6}{56x+16y}\)
\(\Rightarrow\)\(\dfrac{1,6}{56x+16y}=\dfrac{0,02}{x}\)
\(\Leftrightarrow1,6x=1,12x+0,32y\)
\(\Leftrightarrow0,48x=0,32y\)
\(\Leftrightarrow\)\(\dfrac{x}{y}=\dfrac{0,32}{0,48}=\dfrac{2}{3}\Rightarrow x=2;y=3\)
CT của oxit: Fe2O3