Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tính hoá trị của các nguyên tố trong các hợp chất sau:
a/ S trong hợp chất SO3
\(\overset{\left(x\right)}{S}\overset{\left(II\right)}{O_3}\Rightarrow ADquytắchóatrị:x.1=\left(II\right).3\\ \Rightarrow x=VI\)
b/ P trong hợp chất P2O5\
\(\overset{\left(x\right)}{P_2}\overset{\left(II\right)}{O_5}\Rightarrow ADquytắchóatrị:x.2=\left(II\right).5\\ \Rightarrow x=V\)
c/ Al trong hợp chất Al2(SO3)4 biết SO4(ll)
\(\overset{\left(x\right)}{Al_2}\overset{\left(II\right)}{\left(SO_4\right)_3}\Rightarrow ADquytắchóatrị:x.2=\left(II\right).3\\ \Rightarrow x=III\)
d/ Ca trong hợp chất Ca (OH)2 (OH)(l)
\(\overset{\left(x\right)}{Ca}\overset{\left(I\right)}{\left(OH\right)_2}\Rightarrow ADquytắchóatrị:x.1=\left(I\right).2\\ \Rightarrow x=II\)

Câu I:
H(I) và Br(I), H(I) và S(II), N(III) và H(I), Si(IV) và H(I), H(I) và SO4 (II), H(I) và PO4(III), H(I) và NO3(I), Na(I) và O(II), Ba(II) và O(II), Al(III) và O(II), C(IV) và O(II), S(VI) và O(II), P(V) và O(II)

Câu 6. \(P_2O_3\\ NH_3\\ FeO\\ Cu\left(OH\right)_2\\ Ca\left(NO_3\right)_2\\ Ag_2SO_4\\ Ba_3\left(PO_4\right)_2\\ Fe_2\left(SO_4\right)_3\\ Al_2\left(SO_4\right)_3\\ NH_4NO_3\)
Câu 5 : \(NO:N\left(II\right),O\left(II\right)\\ NO_2:N\left(IV\right),O\left(II\right)\\N_2O_3:N\left(III\right),O\left(II\right) \\ N_2O_5:N\left(V\right),O\left(II\right)\\ NH_3:N\left(III\right),H\left(I\right)\\ HCl:H\left(I\right),Cl\left(I\right)\\ H_2SO_4:H\left(I\right),SO_4^{2-}:\left(II\right)\\ H_3PO_4:H\left(I\right),PO_4\left(III\right)\\ Ba\left(OH\right)_2:Ba\left(II\right),OH\left(I\right)\\ Na_2SO_4:Na\left(I\right),SO_4\left(II\right)\\ NaNO_3:Na\left(I\right),NO_3\left(I\right)\\ K_2CO_3:K\left(I\right),CO_3\left(II\right)\\ K_3PO_4:K\left(I\right),PO_4\left(III\right)\\ Ca\left(HCO_3\right)_2:Ca\left(II\right),HCO_3\left(I\right)\)

CaCO3 có PTK =100g/mol
=> %Ca=\(\frac{40}{100}.100=40\%\)
%C=12:100.100=12%
%O=3.16:100.100=48%
H2SO4 có PTK =98
=> %H=2.1:98.100=2%
%S=32:98.100=32,7%
=> %O=100-2-32,7=65,3%
Fe2O3 có PTK =160
=> %Fe=56.2:160.100=70%
=> %O=100-70=30%
Mg(OH)2 có PTK: 58g/mol
=> %Mg=24:56.100=42,9%
%H=1.2:56.100=3,6%
=> %O=100-42,9-3,6=56,5%

câu 1
HBr
đặt b là hóa trị của Br
1.I=1.b
b=I
=>hóa trị của Br=I
tương tự như các ý còn lại

Em ơi trong những bài này anh nghĩ bài nào em cũng cần. Nhưng em làm được bài nào chưa? Bài em muốn được hỗ trợ nhất là bài nào?

\(PTK_{NaNO_3}=23+14+3.16=85\left(đvC\right)\)
\(\%m_{Na}=\dfrac{23}{85}.100=27,05\%\)
\(\%m_N=\dfrac{14}{85}.100=16,47\%\)
\(\%m_O=\dfrac{3.16}{85}=56,47\%\)
\(PTK_{K_2CO_3}=2.39+12+3.16=138\left(đvC\right)\)
\(\%m_K=\dfrac{78}{138}.100=56,52\%\)
\(\%m_C=\dfrac{12}{138}.100=8,69\%\)
\(\%m_O=\dfrac{3.16}{138}.100=34,78\%\)
các ý còn lại làm tương tự
bạn cho mik thêm chỗ này nhé, lúc đấy vội nên mik ghi thiếu
\(\%m_O=\dfrac{3.16}{85}.100=56,47\%\)
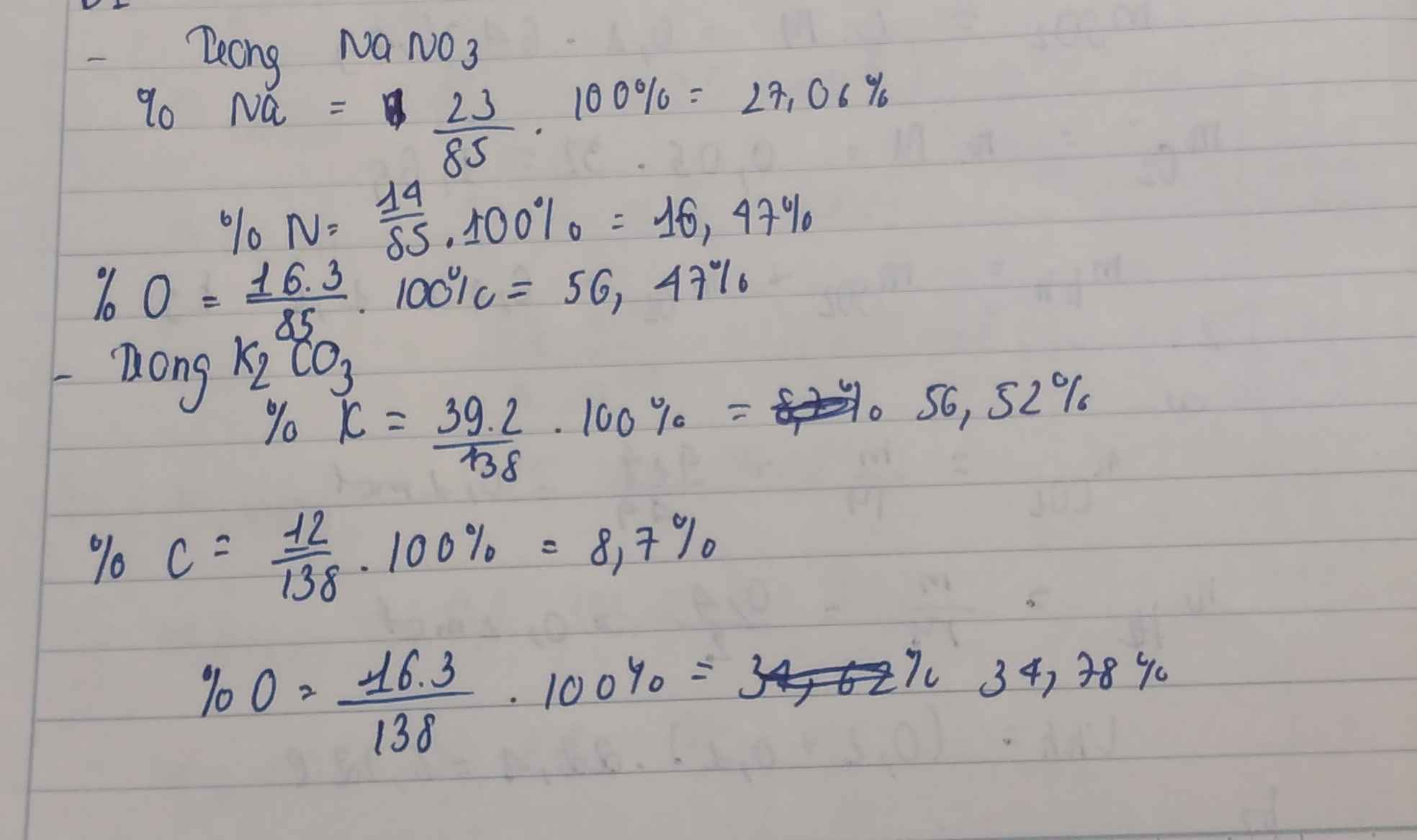
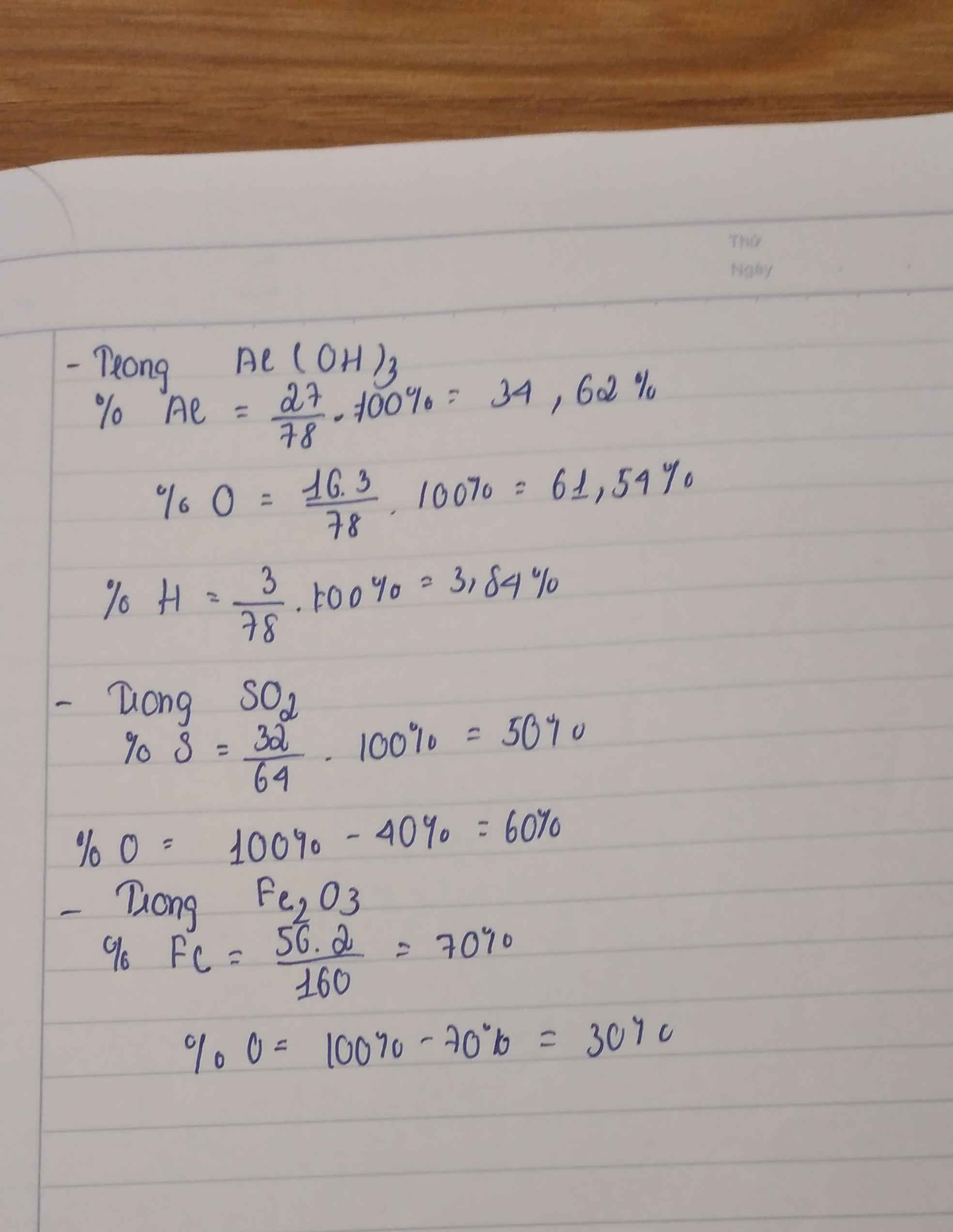
1, \(M_{H_2SO_4}=1.2+32+16.4=98g/mol\)
\(\%H=\frac{1.2}{98}.100\%\approx2,04\%\)
\(\%S=\frac{32}{98}.100\%\approx32,65\%\)
\(\%O=100\%-2,04\%-32,65\%=65,31\%\)
2, \(M_{CH_3COOH}=12+1.3+12+16+16+1=60g/mol\)
\(\%C=\frac{12.2}{60}.100\%=40\%\)
\(\%H=\frac{1.4}{60}.100\%\approx6,67\%\)
\(\%O=1005-40\%-6,67\%=53,33\%\)
3, \(M_{NH_3}=14+1.3=17g/mol\)
\(\%m_N=\frac{14}{17}.100\%=82,35\%\)
\(\%m_H=\frac{3.1}{17}.100\%=17,65\%\)
4, \(M_{SO_2}=32+16.2=64g/mol\)
\(\%m_S=\frac{32}{64}.100\%=50\%\)
\(\%m_O=\frac{16.2}{64}.100\%=50\%\)
5, \(M_{SO_3}=32+16.3=80g/mol\)
\(\%S=\frac{32.100}{80}=40\%\)
\(\%O=100\%-40\%=60\%\)
6, \(M_{NH_4NO_3}=14.2+1.4+16.3=80g/mol\) (Đã sửa đề)
\(\%N=\frac{14.2.100}{80}=35\%\)
\(\%H=\frac{4.100}{80}=5\%\)
\(\%O=100\%-35\%-5\%=60\%\)