Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Zn + 2HCl ---> ZnCl2 + H2
b, nZn=\(\dfrac{13}{65}=0,2mol\)
Ta có: 1 mol Zn ---> 1 mol H2
nên 0,2 mol Zn ---> 0,2 mol H2
VH2=0,2.22,4=4,48 mol

a) \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
nZn = \(\dfrac{13}{65}=0,2mol\)
Theo pt: nH2 = nZn = 0,2 mol
=> VH2 = 0,2.22,4 = 4,48 lít
b) Theo pt: nZnCl2 = nZn = 0,2 mol
=> mZnCl2 = 0,2.136 = 27,2g

\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,4 0,2 ( mol )
\(m_{HCl}=0,4.36,5=14,6g\)
\(m_{ddHCl}=\dfrac{14,6\times100}{14,6}=100g\)
\(m_{ddspứ}=100+13=113g\)
\(m_{ZnCl_2}=0,2.136=27,2g\)
\(C\%_{ZnCl_2}=\dfrac{27,2}{113}.100=24,07\%\)

\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,5 0 0
0,2 0,4 0,2 0,2
0 0,1 0,2 0,2
Sau phản ứng, axit HCl còn dư và dư \(m=0,1\cdot36,5=3,65g\)
\(m_{ZnCl_2}=0,2\cdot136=27,2g\)
\(V_{H_2}=0,2\cdot22,4=4,48l\)

a, \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Zn + 2HCl -----> ZnCl2 + H2
0,2 0,4 0,2 0,2
b, \(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
\(a,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,2<--0,4<--------0,2<---0,2
\(b,\left\{{}\begin{matrix}m_{Zn}=0,1.65=13\left(g\right)\\m_{HCl}=0,4.36,5=14,6\left(g\right)\end{matrix}\right.\\ c,m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)

\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2....................0.2..........0.2\)
\(m_{ZnCl_2}=0.2\cdot136=27.2\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)

\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2.......0.4.......................0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\)
\(C\%_{HCl}=\dfrac{0.4\cdot36.5}{200}\cdot100\%=7.3\%\)
\(n_{CuO}=\dfrac{24}{80}=0.3\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(1..........1\)
\(0.3.........0.2\)
\(LTL:\dfrac{0.3}{1}>\dfrac{0.2}{1}\Rightarrow CuOdư\)
\(m_{CuO\left(dư\right)}=\left(0.3-0.2\right)\cdot64=6.4\left(g\right)\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{ZnCl_2}=n_{Zn}=n_{H_2}=0,15\left(mol\right);n_{HCl}=2.0,15=0,3\left(mol\right)\\ a,m=m_{Zn}=0,15.65=9,75\left(g\right)\\ b,C_{MddHCl}=\dfrac{0,3}{0,15}=0,2\left(l\right)\\ c,m_{ZnCl_2}=0,15.136=20,4\left(g\right)\)

Mình thay trên câu a luôn nhé.
5. Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
a) Ta có PTHH :
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,1 mol 0,2 mol 0,1 mol 0,1 mol
Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
b) Khối lượng của FeCl2 tạo thành sau p.ứng là :
mFeCl2 = 0,1.127 = 12,7 (g)
c) Thể tích khí Hiđro (đktc) tạo thành sau p.ứng là :
VH2 = 0,1.22,4 = 2,24 (l)
4. Công thức của B là : NaxCyOz
+ \(m_{Na}=\frac{106.43,6}{100}\approx46\left(g\right)\)
\(m_C=\frac{106.11,3}{100}\approx12\left(g\right)\)
\(m_O=\frac{106.45,3}{100}\approx48\left(g\right)\)
+ \(n_{Na}=\frac{46}{23}=2\left(mol\right)\)
\(n_C=\frac{12}{12}=1\left(mol\right)\)
\(n_O=\frac{48}{16}=3\left(mol\right)\)
Suy ra trong một p.tử h/c có 2 n.tử Na, 1 n.tử C và 3 n.tử O.
\(\Rightarrow\) CTHH của hợp chất B là Na2CO3.

a, nH2=5,6/22,4=0,25 mol
Zn+2HCl->ZnCl2+H2
0,25 0,5 0,25 0,25
mZn pư=0,25.65=16,25 g
b, C%HCl=0,5.36,5.100/200=9,125%
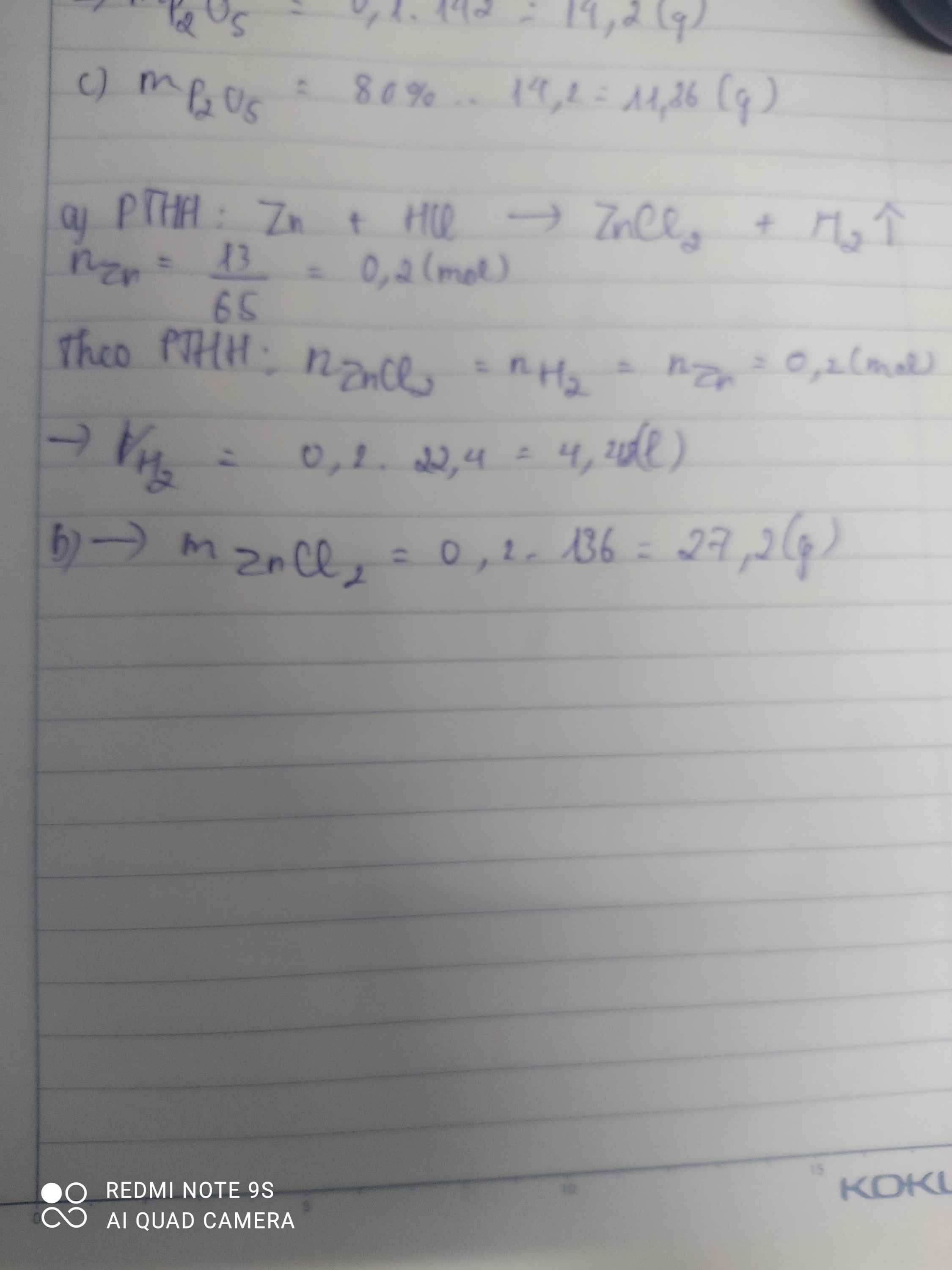
a) $n_{HCl} = \dfrac{18,25.50\%}{36,5} = 0,25(mol)$
$Zn + 2HCl \to ZnCl_2 + H_2$
Theo PTHH :
$n_{Zn\ pư} = n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,125(mol)$
$m_{Zn\ pư} = 0,125.65 = 8,125(gam)$
$V_{H_2} = 0,125.22,4 = 2,8(lít)$
b)
$m_{dd\ sau\ pư} = 8,125 + 18,25 - 0,125.2 = 26,125(gam)$
$C\%_{ZnCl_2} = \dfrac{0,125.136}{26,125}.100\% = 65,1\%$