Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nKOH = 0,007/56 = 1,25.10-4 mol
C17H35COOH + KOH -> C17H35COOK + H2O
1,25.10-4 <- 1,25.10-4
mC17H35COOH = 1,25.10-4 . 284 = 0,0355g
mtrieste glixerol/ 1g chất béo = 1 - 0,0355 = 0,9645g
(C17H35COO)3C3H5 + 3KOH -> 3C17H35COOK + C3H5(OH)3
890 168
0,9645 tam suất mình đc mKOH = 182mg
ΣmKOH = 7 + 182 = 189mg
=> chỉ số xà phòng hóa chất béo là 189 nhe bạn

Chọn đáp án B
• mKOH để trung hòa axit béo tự do = 1000 x 7 = 7000 mg = 7 gam → nKOH = 0,125 mol.
nNaOH = 3,2 mol → nxà phòng hóa = 3,2 - 0,125 = 3,075 mol.
Giả sử triglixerit và axit béo tự do trong chất béo lần lượt là (RCOO)3C3H5 và RCOOH
(RCOO)3C3H5 + 3NaOH 3RCOONa + C3H5(OH)3
-----------------------3,075 mol-------------------1,025 mol
RCOOH + NaOH → RCOONa + H2O
-------------0,125-------------------0,125
Theo BTKL: mRCOONa = mchất béo + mNaOH - mH2O - mC3H5(OH)3 = 1000 + 3,2 x 40 - 0,125 x 18 - 1,025 x 92 = 1031,45 gam

\(n_{H^+}=n_{OH^-}=0,003.0,1=3.10^{-4}\left(mol\right)\)
\(m_{KOH}=3.10^{-4}.56=0,0168\left(g\right)\)
\(0,0168\left(g\right)KOH\rightarrow2,8\left(g\right)chấtbeo\\ x\left(g\right)KOH\rightarrow1\left(g\right)chấtbeo\)
=> \(x=\dfrac{0,0168.1}{2,8}=6,10^{-3}\left(g\right)=6\left(miligam\right)\)
Vậy chỉ số của mẫu axit trên là 6

Số mol KOH là: nKOH = 0,003. 0,1 = 0,0003 (mol)
Khối lượng KOH cần dùng là mKOH = 0,0003.56 = 0,0168 (g) = 16,8 (mg)
Trung hòa 2,8 gam chất béo cần 16,8 mg KOH
⇒ Trung hòa 1 gam chất béo cần x mg KOH
⇒ x = 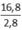 = 6
= 6
Vậy chỉ số axit của mẫu chất béo trên là 6.

Chọn đáp án C
mKOH cần để trung hòa lương axit béo là 265,2 × 7 = 1856,4 (g)
→ nKOH = 33,15 (mol) → nNaOH cần để trung hòa lượng axit béo bằng = 33,15 (mol)
nNaOH = 213,15 (mol) → số mol NaOH tham gia phản ứng xà phòng hóa = 180 (mol)
→ nGlyxerol = 60 (mol) → mglyxerol = 5520 (g) = 5,52 (kg)

Chọn đáp án A
n N a O H =639,45 mol. Từ chỉ số axit suy ra n K O H = 99 , 45 m o l = n N a O H cần để phản ứng với lượng axit béo tự do, suy ra nNaOH phản ứng với triglixerit là: 639,45-99,45=540 mol, suy ra n G l i x e r o l = 180 m o l ⇒ m g l i x e r o l = 16 , 56 k g

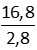 = 6
= 6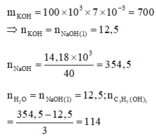
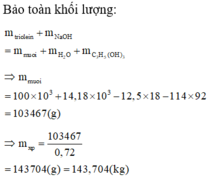
Chọn đáp án B
Chỉ số axit chính là số milig KOH trung hòa hết 1g chất béo
1g chất béo----------5,6mg KOH
5g chất béo----------xKOH
Suy ra x=28mgKOH vì thay thế NaOH bằng KOH nên
để phản ứng hết
n N a O H = n K O H = 28 56 = 0 , 5 milimol
⇒ m N a O H 30 % = 0 , 5 . 40 . 100 30 = 66 , 67 ( m g )