Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 2:
a) CO2 +Ba(OH)2---->BaCO3 +H2O
b)n CO2 =0,1
nCO2 = nBa(OH)2 =0,1
----->Cm =0,5M
c)nCO2 = nBa(OH)2 =0,1
--->mBa(OH)2 =17,1
câu 1:
Khí SO2 và CO2 do nhà máy thải ra gây ô nhiễm ko khí rất nặng. Vì vậy, để loại bỏ bớt lượng khí trên trước khi thải ra môi trường ta cần cho những khí này qua nước vôi trong ( Ca(OH)2 ) để chúng được hấp thụ lại và tạo ra sản phẩm là những chất không ảnh hưởng tới môi trường
Ca(OH)2+ CO2-> CaCO3 + H2O
Ca(OH)2+ SO2-> CaSO3 + H2O

1) + Lấy mỗi chất 1 lượng xác định và đánh dấu.
+ Cho các chất td với dd HCl dư:
- Nếu xuất hiện kết tủa trắng: Ag2O
Ag2O + 2HCl \(\rightarrow\) 2AgCl \(\downarrow\) + H2O
- Nếu tạo dd màu xanh lam: CuO
CuO + 2HCl \(\rightarrow\) CuCl2 + H2O
- Nếu có khí thoát ra, mùi hắc: MnO2
MnO2 + 4HCl \(\rightarrow\) MnCl2 + Cl2 + 2H2O

1. nH2=3.36/22.4=0.15mol
PT: Fe+ 2HCl ---> FeCl2 + H2
0.15 0.3 0.15
a)mFe=0.15*56=8.4g
b)CMddHCl = 0.3/0.5=0.6M
2. nCO=15.68/22.4=0.7 mol
Đặt x,y lần lượt là số mol của CuO,Fe2O3 :
PT: CuO+ CO ---> Cu + CO2
x x
Fe2O3 + 3CO --> Fe + 3CO2
y 3x
Theo pthh,ta lập được hệ pt:
80x + 160y=40(1)
x + 3x = 0.7 (2)
giải hệ pt trên,ta được :x =0.1, y=0.2
Thế x,y vào PTHH:
CuO+ CO ---> Cu + CO2
0.1 0.1
Fe2O3 + 3CO --> Fe + 3CO2
0.2 0.6
mCuO=0.1*80=8g => %CuO=(8/40)*100=20%
=>%Fe2O3= 100 - 20=80%
b) Để tách Cu ra khỏi hỗn hợp Fe,Cu.Dùng nam châm để hút sắt ra khỏi hỗn hợp (sắt có tính từ),còn lại là đồng.
Chúc em học tốt !!@

a) cho hỗn hợp đi qua dung dịch Ca(OH)2 dư thu được khí CO
Ca(OH)2+CO2=>CaCO3+H2O
lọc lấy kết tủa nung đến khối lượng không đổi sẽ thu được lại CO2
b) cho tác dụng với C trong đk có không khí
c) đốt cháy hỗn hợp trong khí oxi
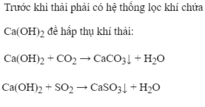



Để loại bỏ được CO2 , SO2 ta dùng một chất vô cùng rẻ và dể tìm kiếm là : Ca(OH)2 để hấp thụ lại và tạo ra những chất không gây ô nhiễm môi trường.
CO2 + Ca(OH)2=> CaCO3 + H2O
SO2 + Ca(OH)2 => CaSO3 + H2O