Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1,
- Xét phần 2:
\(n_{CH_3COOC_2H_5}=\dfrac{4,4}{88}=0,05\left(mol\right)\)
PTHH: CH3COOH + C2H5OH \(\xrightarrow[t^o]{H_2SO_{4\left(đ\right)}}\) CH3COOC2H5 + H2O
LTL: 0,5a < 0,5b (do a < b) => C2H5OH dư
Theo pthh: \(n_{CH_3COOH\left(pư\right)}=n_{CH_3COOC_2H_5}=0,05\left(mol\right)\)
Mà H = 50%
=> \(n_{CH_3COOH\left(bđ\right)}=\dfrac{0,05}{50\%}=0,1\left(mol\right)\)
Xét phần 2:
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
2CH3COOH + 2Na ---> 2CH3COONa + H2
0,1--------------------------------------------->0,05
2C2H5OH + 2Na ---> 2C2H5ONa + H2
0,4<----------------------------------------0,2
=> Trong X có: \(\left\{{}\begin{matrix}n_{CH_3COOH}=0,1.2=0,2\left(mol\right)\\n_{C_2H_5OH}=0,4.2=0,8\left(mol\right)\end{matrix}\right.\)
2, Gọi \(\left\{{}\begin{matrix}n_{CH_3COOH}=a\left(mol\right)\\n_{C_2H_5OH}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(n_{H_2O}=\dfrac{23,4}{18}=1,3\left(mol\right)\)
PTHH:
CH3COOH + 2O2 --to--> 2CO2 + 2H2O
a------------------------------------------>2a
C2H5OH + 3O2 --to--> 2CO2 + 3H2O
b-------------------------------------->3b
=> Hệ pt \(\left\{{}\begin{matrix}60a+46b=25,8\\2a+3b=1,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\left(TM\right)\)
PTHH: \(CH_3COOH+C_2H_5OH\xrightarrow[t^o]{H_2SO_{4\left(đ\right)}}CH_3COOC_2H_5+H_2O\)
LTL: 0,2 < 0,3 => Rượu dư
Theo pthh: \(n_{CH_3COOH\left(pư\right)}=n_{CH_3COOC_2H_5}=\dfrac{14,08}{88}=0,16\left(mol\right)\)
=> \(H=\dfrac{0,16}{0,2}.100\%=80\%\)

Phần 2:
nH2 = 0,03 => nAl dư = 0,02
nNaOH = nAl dư + 2nAl2O3 => nAl2O3 = 0,08
Phần 1:
nAl dư = 0,02k; nAl2O3 = 0,08k; nFe = a
=> 0,02k.27 + 0,08k.102 + 56a = 9.39
nH2 = 0.02k.1,5 + a = 0,105
k = 0.5 và a = 0,09
Fe : O = a : (0,08k.3) => Fe3O4
m2 = 9,39 + 9,39/k =28,17g

2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
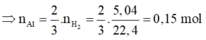
⇒ m F e 2 O 3 (bđ) = 20,05 - 0,15.27 = 16g
⇒ n F e 2 O 3 (bđ) = 16/160 = 0,1 mol
2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
Bđ: 015 0,1
Pư: 0,15 0,065
Dư: 0 0,025
⇒ m F e 2 O 3 (dư) = 0,025.160=4g
⇒ Chọn A.

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
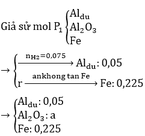
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
a 0,5a
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
b 0,5b
b) Gọi a là số mol của Na
b là số mol của K
\(m_{Na}+m_K=10,1\left(g\right)\)
⇒ \(n_{Na}.M_{Na}+n_K.M_K=10,1g\)
⇒ 23a + 39b = 10,1g (1)
Theo phương trình : 0,5a + 0,5b = 0,15(2)
Từ(1),(2), ta có hệ phương trình :
23a + 39b = 10,1g
0,5a + 0,5b = 0,15
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
\(m_{Na}=0,1.23=2,3\left(g\right)\)
\(m_K=0,2.39=7,8\left(g\right)\)
0/0Na = \(\dfrac{2,3.100}{10,1}=22,77\)0/0
0/0K = \(\dfrac{7,8.100}{10,1}=77,23\)0/0