Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tổng hạt mang điện `AB_3^{2-}` là `82`
`->2p_A+3.2p_B+2=82(1)`
Số hạt mang điện trong hạt nhân `A` hơn `B` là `8`
`->p_A-p_B=8(2)`
`(1)(2)->p_A=16(S);p_B=8(O)`
`Z_A=16`
`Z_B=8`

Đáp án A
Theo giả thiết ta có: 2 Z X + 6 Z Y + 2 = 82 Z X - Z Y = 8 ⇒ Z X = 16 Z Y = 8

1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl

Ta có :
$2p_A + n_A + 2p_B + n_B = 177$
$(2p_A + 2p_B) - (n_A + n_B) = 47$
Suy ra: $2p_A + 2p_B = 112(1)$
Mà: $2p_B - 2p_A = 8(2)$
Từ (1)(2) suy ra $p_A = 26 ; p_B = 30$
bạn có thể giải thích ở chỗ tại sao ra 2pA+2pB=112 được không
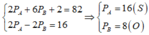
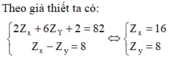
Ta có: P = E (Do nguyên tử trung hòa về điện)
- Tổng số hạt mang điện trong AB32- là 82.
⇒ 2PA + 3.2PB = 82 - 2 (1)
- Số hạt mang điện trong nhân nguyên tử A nhiều hơn trong nguyên tử B là 8.
⇒ PA - 2PB = 8 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P_A=16=Z_A\\P_B=8=Z_B\end{matrix}\right.\)
Vậy: Số hiệu nguyên tử A và B lần lượt là 16 và 8.